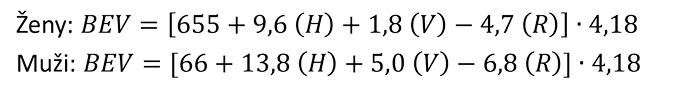Základní složky výživy
Základní složky stravy se označují jako živiny (nutrienty). Dělí na makronutrienty a mikronutrienty. Makronutrienty jsou nositeli energie, proto jsou někdy také označovány jako kalorifery. Patří mezi ně proteiny (bílkoviny), lipidy (tuky), sacharidy (cukry a škroby), alkohol. Oxidací těchto živin se získá z 1 g bílkovin, stejně jako z 1 g sacharidů 17 kJ (4,1 kcal), z 1 g tuků 37 kJ (9 kcal), z 1 g alkoholu 29 kJ (7 kcal).
Jejich doporučovaný tzv. „energetický trojpoměr základních živin“ znamená, že na celkovém energetickém příjmu (CEP) by se měly u zdravých dospělých osob s obvyklou fyzickou aktivitou proteiny podílet 12–15 %, lipidy maximálně do 30 % a sacharidy zbylými 55–65 %. To představuje zhruba poměr 1 gramu bílkoviny k 1 g lipidů a 4 g sacharidů. U kojených dětí a batolat toto pravidlo neplatí. V mateřském mléce tvoří energie z lipidů až 50 % energie celkové. Rovněž výjimku tvoří sportovci s extrémní fyzickou zátěží, kde vzhledem k energetickým nárokům je někdy nutno zvýšit energetickou denzitu stravy zvýšeným podílem tuků.
Mikronutrienty dělíme na vitaminy a minerální látky. Ty se podle přijímaného množství dělí na makroelementy (přijímány v dávkách větších než 100 mg denně), mikroelementy (přijímány v množství od 1 do 100 miligramů denně) a stopové prvky (mikrogramové dávky denně).
Energie
Všechny životní procesy jsou spojeny s transformacemi energie. Zelené rostliny ji přijímají formou světelné energie, heterotrofní organismy pak v podobně energie chemické. Energie je vracena okolí v degradované formě energie tepelné nebo ve formě energie chemické v organických sloučeninách s nižším obsahem energie. Energie je definována jako míra různých forem pohybu hmoty. Mezinárodní jednotkou SI je 1 joule (J). Dřívější a někde dosud používaná je jednotka práce kalorie (1 cal = 4,18 J), která vyjadřuje množství tepla, potřebného k ohřátí 1 g vody o 10 C, z 150 C na 160 C. Člověk jako všechny heterotrofní organismy přijímá energii ve formě energie chemické, uložené v makronutrientech potravy. Při jejich štěpení se energie ukládá ve formě pro organismus rychle použitelných makroergních vazeb typu adenosintrifosfátu (ATP). Energie je nezbytná pro životní procesy, jako jsou biosyntézy a reparace, svalové kontrakce, udržení membránových potenciálů apod. Hlavní metabolickou cestou tvorby ATP je aerobní oxidace mastných kyselin (MK) a glukózy. V tomto procesu zároveň dochází k přeměně průměrně 60 % původně přijaté chemické energie na energii tepelnou. Pro krátkodobé potřeby produkce ATP může člověk využít i anaerobní oxidace glukózy za vzniku laktátu. Tato metabolická cesta je však kapacitně omezená a z hlediska celkového energetického obratu nepříliš významná. Celkový energetický výdej organismu v konečné podobě znamená výdej tepla organismem při měřitelné spotřebě kyslíku a produkci oxidu uhličitého (Obrázek 1).
Změny tepelné energie se měří kalorimetricky.
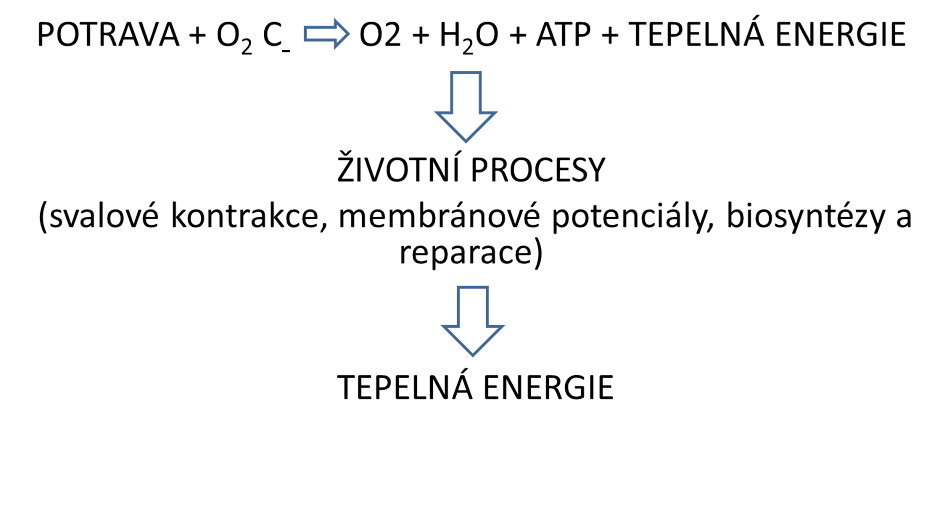
Obrázek 1: Zjednodušené schéma energetického výdeje
Souhrn oxidace makronutrientů (převzato podle (1)):
Glukóza
- 1 g glukózy + 0,747 l O2 = 0,747 l CO2 + 0,6 g H2O + 15,15 kJ
- RQ = 1,0
- energetický obsah = 15,56 kJ
- uvolnění energie = 20,83 kJ/l O2
Triacylglyceroly
- 1 g triacylglycerolů + 2,023 l O2 = 1,436 l CO2 + 1,07 g H2O + 39,63 kJ
- RQ = 0,71
- energetický obsah = 39,63 kJ
- uvolnění energie = 19,59 kJ/l O2
Protein
- 1 g proteinu + 1,031 l O2 = 0,859 l CO2 + 0,403 g H2O + (urea, HN3, kreatinin) + 19,72 kJ
- RQ = 0,833
- energetický obsah = 19,72 kJ
- uvolnění energie = 19,13 kJ/l O2
Těsný vztah mezi energetickým výdejem a metabolickými procesy vysvětluje používání termínů „energetický výdej“ (energy expenditure) a „metabolická rychlost“ (metabolic rate) jako synonym. Z hlediska skladby celkového energetického výdeje se rozlišuje:
Bazální termogeneze (bazální energetický výdej)
Jde o energii potřebnou pro zachování základních vitálních funkcí (udržení membránového potenciálu, klidové kardio-respirační funkce, bazální rychlosti obratu proteinů, udržování tělesné teploty apod.) včetně růstu. V literatuře je tato energie označována jako bazální energetický výdej (BEV) nebo bazální metabolická rychlost (BMR). Obvykle tvoří největší část celkového energetického výdeje (CEV). Závisí na velikosti tzv. netučné tělesné hmoty (fat-free mass, FFM), na které se podílejí zejména viscerální orgány a svalstvo. Průměrná hodnota BEV je 90 J/kg FFM. Zastoupení netučné tělesné hmoty je určeno genetickými dispozicemi a fyzickou trénovaností jedince. Orientačně se dá odhadnout podle velikosti těla (tělesná hmotnost a tělesná výška, event. tělesný povrch), stáří a pohlaví jedince. BEV je dále ovlivněn hormonálními vlivy, zejména hormony štítné žlázy, adrenalinem. Je zvýšen u akutních stresových stavů (polytraumata, popáleniny, sepse, pooperační stavy), po léčbě některými léky, při zvýšení tělesné teploty.
Na principu odhadu velikosti FFM je založena celá řada výpočtů jak BEV, tak tzv. klidového energetického výdeje (KEV), tj. celkového energetického výdeje zmenšeného o energetické nároky na fyzickou aktivitu. Nejznámější a zároveň jednou z prvních je Hariss-Benedictova rovnice.
Výpočet bazálního energetického výdeje podle Harris-Benedictovy rovnice:
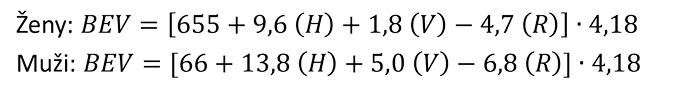
(BEV = bazální energetický výdej (kJ/den), H = tělesná hmotnost (kg), V = tělesná výška (cm), R = věk (roky))
Při krajních hodnotách tj. při tělesné hmotnosti pod 40 kg či nad 120 kg dochází ke zkreslení výpočtu.
Tabulka 1: Výpočet klidového energetického výdeje podle tělesné hmotnosti (TH).
Výsledky jsou uvedeny v kcal. (1 kcal = 4,18 kJ). Převzato podle (2). R* korelační koeficient měřených BEV a predikovaných hodnot, SD** směrodatná odchylka rozdílů mezi aktuální a počítanou hodnotou
|
Pohlaví a věková skupina
|
Rovnice pro výpočet KEV z tělesné hmotnosti (TH)
|
R*
|
SD**
|
|
Muži
|
|
|
|
|
0–3
|
(60,9 * TH) – 54
|
0,97
|
53
|
|
3–10
|
(22,7 * TH) + 495
|
0,86
|
62
|
|
10–18
|
(17,5 * TH) + 651
|
0,90
|
100
|
|
18–30
|
(15,3 * TH) + 679
|
0,65
|
151
|
|
30–60
|
(11,6 * TH) + 879
|
0,60
|
164
|
|
> 60
|
(13,5 * TH) + 487
|
0,79
|
148
|
|
Ženy
|
|
|
|
|
0–3
|
(61.0 * TH) – 51
|
0,97
|
61
|
|
3–10
|
(22,5 * TH) + 499
|
0,85
|
63
|
|
10–18
|
(12,2 * TH) + 746
|
0,75
|
117
|
|
18–30
|
(14,7 * TH) + 496
|
0,72
|
121
|
|
30–60
|
(8,7 * TH) + 829
|
0,70
|
108
|
|
> 60
|
(10,5 * TH) + 596
|
0,74
|
108
|
K tomuto výpočtu je třeba přidat energetickou potřebu pro fyzickou aktivitu.
Termogeneze spojená s fyzickou aktivitou (Energetický výdej spojený s fyzickou aktivitou)
Obvykle druhou největší položkou celkového energetického výdeje je energie nutná pro krytí nároků spojených s fyzickou aktivitou. Z hlediska náročnosti se rozlišují následné kategorie fyzické aktivity.
Tabulka 2: Kategorizace energetických nároků podle typu fyzické aktivity, vyjádřené faktorem fyzické aktivity (FFA), který se vztahuje ke KEV. Převzato podle (3).
|
Kategorie fyzické aktivity
|
Faktor fyzické aktivity (FFA)
|
|
Odpočinek (spaní, ležení)
|
1
|
|
Lehká (sedavý způsob: řidič, sekretářka, student)
|
1,3
|
|
Středně těžká (zdravotní sestra, prodavačka)
|
2,5
|
|
Těžká (v hutích, přenášení těžkých břemen)
|
5
|
|
Velmi těžká (dřevorubci, pracovníci v lomech, kopáč s krumpáčem)
|
7
|
Pro podrobnější výpočet lze konkretizovat odhad denní potřeby energie podle počtu hodin a typu fyzické aktivity podle následujícího postupu:
- výčet jednotlivých kategorií aktivit (viz výše) s uvedením doby trvání během jednoho dne (celkem 24 hodin).
- vynásobení počtu hodin trvání každé aktivity odpovídajícím faktorem fyzické aktivity (FFA)
- vydělení součtu všech násobků 24 (obdržení průměrného FFA/24 hodin)
- vynásobení průměrného FFA/24 hodin hodnotou klidového energetického výdeje (obdržení odhadu celkového energetického výdeje CEV)
Energetickou náročnost vybraných druhů fyzické aktivity v porovnání se spánkem u 70 kg jedince dokumentuje Tabulka 3. V současné době převažuje u mnoha lidí populace sedavý způsob života, kdy energetický výdej spojený s fyzickou aktivitou představuje pouze kolem 30 % celkového energetického výdeje.
Tabulka 3: Příklady energetických nároků na fyzickou aktivitu. Hodnoty jsou uvedeny v kJ/min pro neobézního 70 kg jedince. Převzato podle (3).
|
KJ/min
|
|
Spánek
|
4,5
|
|
Sezení
|
5
|
|
Stání
|
6
|
|
Rychlá chůze (6,4 km/hod)
|
30
|
|
Běh (8 km/hod)
|
43
|
|
Jízda na kole (16 km/hod)
|
30
|
|
Plavání (25 m/min)
|
28
|
Při hrubém odhadu celkové energetické potřeby dospělých zdravých osob se lze orientovat podle následujících doporučení uvedených v Tabulka 4.
Tabulka 4: Hrubý odhad celkové energetické potřeby zdravých dospělých osob podle druhu převažující fyzické aktivity.
|
Druh převažující fyzické aktivity
|
Pomocná kalkulace
|
Muži
|
Ženy
|
|
Lehká
|
Základ
|
9,5–12 MJ
(2300–2900 kcal)
|
8–9 MJ
(1900–2200 kcal)
|
|
Středně těžká
|
Základ + 2,5 MJ (600 kcal)
|
12–14,5 MJ
(2900–3500 kcal)
|
10,5–11,5 MJ
(2900–3500 kcal)
|
|
Těžká
|
Základ + 5 MJ (1200 kcal)
|
14,5–17 MJ
(3500–4100 kcal)
|
13–14 MJ
(3100–3400 kcal)
|
Dietou indukovaná termogeneze (Energetický výdej spojený s utilizací živin)
Jde o ztráty energie, které jsou spojeny s příjmem potravy a jsou nutné pro trávení, vstřebávání a utilizaci živin. Představují kolem 10 % celkového energetického výdeje.
Označují se také jako termický účinek potravy či v minulosti specificko-dynamický účinek potravy. Jejich velikost je ovlivněna skladbou a velikostí potravy a je pravděpodobně závislá na velikosti hepatické glukoneogeneze, humorálně řízené především inzulinem a glukagonem.
Regulační termogeneze (měří se společně s Bazálním energetickým výdejem)
Jedná se o změny v produkci tepla (poměr produkce chemické a termické energie), které se podílejí na regulaci tělesné teploty a tělesné váhy. Tato v podstatě adaptační schopnost organismu šetří či naopak proplýtvává energii ve formě tepla při změně teploty okolního prostředí, či při nerovnováze mezi energetickým příjmem a zvyklými potřebami organismu. Významnou roli v ní hraje adrenergní systém, hnědá a bílá tuková tkáň, svalstvo.
Proteiny
Proteiny jsou základní biologické makromolekuly složené z polypeptidových řetězců. Obsahují 100–2000 aminokyselinových zbytků spojených peptidovou vazbou. Pro funkci bílkovin je rozhodující jak řazení jednotlivých, v přírodě se vyskytujících 20 aminokyselin (AMK), tak jejich sekundární, terciální, resp. kvartérní struktura. Proteiny tvoří strukturu živého organismu, jsou nositeli alergenní druhové specificity, jsou zásadní pro transkripci genetické informace obsažené v genové DNA a jako enzymy katalyzují buněčné reakce. Mezi další funkce proteinů patří výživa, molekulární transport, imunita, motilita, regulace metabolismu a řada dalších.
V těle probíhá nepřetržitě degradace a resyntéza bílkovin, společně označované jako proteinový obrat. Jeho rychlost klesá u zdravých lidí s přibývajícím věkem. U novorozenců představuje 17,4 g/kg, ve věku 1 roku 6,9 g/kg, u mladých dospělých 3–4 g/kg a starších dospělých 1,9 g/kg tělesné hmotnosti (4). Rovnováhu mezi degradací a syntézou tělesného proteinu ovlivňuje celá řada faktorů. Inzulin jako anabolický hormon stimuluje syntézu proteinu ve skeletárním svalstvu a inhibuje degradaci jak ve svalech, tak v játrech. Katabolický hormon glukagon stimuluje degradaci proteinu tím, že rychle odpovídá na aktuální potřebu glukózy podporou glukoneogeneze ze svalového proteinu mobilizovaných AMK a z laktátu. Podobně ale pomaleji působí kortizol.
Bílkoviny přijaté stravou se po natrávení a štěpení absorbují ve formě AMK v tenkém střevě. V anabolické fázi se tak zvyšují aktuální zásoby AMK použitelných pro syntézu vlastních proteinů. S ubývajícím přísunem AMK ze stravy dochází k zvyšování degradace vlastního zejména svalového proteinu a použití AMK pro jaterní glukoneogenezi. Během prohlubujícího se nekomplikovaného hladovění dochází během prvního týdne hladovění k adaptačním změnám zpomalujícím svalovou devastaci snížením nároků na jaterní glukoneogenezi náhradním využitím ketolátek jako hlavního oxidačního substrátu. Tím dochází k poklesu oxidace AMK, což se projeví sníženým vylučováním urinárního dusíku. Teprve v terminální fázi prostého hladovění je protein opět rychle štěpen, protože je využíván jako energetický zdroj.
Při patologických stavech jako je poranění, infekce, popáleniny, nádory dochází účinkem tzv. stresových hormonů (glukagonu, kortizolu a adrenalinu) k vystupňování glukoneogeneze s vysokými ztrátami tělesného proteinu. Ztráty dusíku větší než 30 g denně odpovídají ztrátě 1 kg netučné tkáně denně a ohrožují během několika dnů život nemocného. Na stavu se spolupodílí i cytokiny produkované aktivovanými makrofágy (např. tumor nekrotizující faktor TNF), které inhibují svalovou syntézu proteinu při současné stimulaci syntézy jaterního proteinu.
Příjem bílkovin potravou je nezbytným zdrojem dusíku, síry a esenciálních AMK, které si lidský organismus není schopen vytvořit endogenně. Mezi esenciální AMK patří: valin, leucin, izoleucin, fenylalanin (+ tyrosin), lysin, methionin (+ cystein), tryptofan a threonin. Jako podmíněně esenciální se označují AMK, které jsou esenciální pouze za určitých okolností, např. při nepřítomnosti prekurzorů, nezralosti enzymatických systémů, za patologických stavů (Tabulka 5). Plně neesenciální jsou pouze alanin, serin a asparagová kyselina s asparaginem.
Tabulka 5: Dělení AMK
|
Výhradně esenciální
|
Podmíněně esenciální
(stavy, vyžadující zvýšenou potřebu)
|
Prekurzoři podm. esenc.
|
Plně neesenciální
|
|
Valin
|
Cystein
(oxidační stres, nedonošenci)
|
← Methionin, Serin
|
Alanin
|
|
Leucin
|
Tyrosin
(renální selhání)
|
← Fenylalanin
|
Serin
|
|
Isoleucin
|
Arginin
(jaterní nedostatečnost)
|
← Glutamin/Glutamová, Asparagová kyselina
|
Asparagová kyselina,
Asparagin
|
|
Fenylalanin
|
Prolin (uremie, nedonošené děti)
|
← Glutamová kyselina
|
|
|
Lysin
|
Histidin (uremie, děti)
|
← Adenin, Glutamin
|
|
|
Methionin
|
Glycin
|
← Serin, Cholin
|
|
|
Tryptofan
|
Glutamová kyselina (malnutrice)
Glutamin (sepse)
|
|
|
|
Threonin
|
Taurin (nedonošenci, novorozenci)
|
|
|
Při resyntéze proteinů dochází ke ztrátám části AMK oxidačními pochody. Vzniklými metabolickými produkty jsou urea, kreatinin, kyselina močová a další. Měřítkem degradace proteinů je vyloučený dusík. Nejvýznamnější jsou jeho ztráty močí, vylučuje se ale i ve stolici, potu, odloupaných epiteliích, vlasech, nehtech. Aminový dusík představuje 16 % hmotnosti proteinu, proto se dá odhadnout i příjem dusíku z potravy (g) vydělením celkového množství přijatého proteinu (g) konstantou 6,28. Dusíková bilance je rozdíl mezi přijatým a vyloučeným dusíkem. U dětí a lidí v rekonvalescenci by měla být pozitivní dusíková bilance s převažujícím příjmem, nutným ke krytí růstových event. anabolických požadavků, u ostatních dospělých osob nastává za normálních okolností rovnováha mezi příjmem a ztrátami dusíku. Zásoby tělesného proteinu představuje svalový protein a tzv. labilní protein – tj. zásobní jaterní bílkoviny a plazmatický albumin tvořící pouze 1 % tělesného poolu. Z tohoto důvodu se AMK konzumované v nadbytku neskladují (mimo situace tvorby svalu cvičením a růstového období) a jsou zvýšeně degradovány za vzniku urey a ketokyselin, užívaných jako přímý zdroj energie, ke glukoneogenezi a přeměně na tuk.
Z hlediska příjmu bílkovin rozdělujeme bílkoviny podle původu na živočišné a rostlinné, kdy živočišné mají vyšší obsah a zároveň také většinou zastoupení všech esenciálních aminokyselin na rozdíl od bílkovin rostlinného původu. Výživová hodnota každé bílkoviny se určuje pomocí tzv. aminokyselinového skóre, tj. poměrným zastoupením konkrétní, zpravidla esenciální aminokyseliny ve vyšetřované bílkovině ve srovnání s jejím zastoupením v referenčním proteinu. Referenčním proteinem může být např. vaječná bílkovina. Ve smíšené (omnivorní) lidské stravě je z hlediska dostupnosti určující příjem lysinu, dále AMK obsahujících síru (methionin, cystein), threoninu a tryptofanu. Experimentálně byla stanovena jak nezbytná denní množství jednotlivých esenciálních AMK pro zdravého člověka, tak také nejnižší prahová dávka potřebná pro pokrytí obligatorních ztrát dusíku. Činí za podmínek dostatečného energetického příjmu 0,45 g proteinu/kg tělesné hmotnosti. Pro krytí těchto teoreticky vypočítaných minimálních obligatorních ztrát proteinu je potřebný 130–140 % ekvivalent vysoce kvalitních bílkovin stravy což představuje 0,6 g proteinů/kg, den. Jako doporučovaná výživová denní dávka (VDD) pro dospělou zdravou populaci byla proto stanovena hodnota 0,75–0,8 g proteinu /kg tělesné hmotnosti. Proteinová potřeba kojenců do 6 měsíců je 1,73 g/kg tělesné hmotnosti, kolem 1 roku 1,2 g/kg tělesné hmotnosti a u 5–12letých dětí 1 g/kg tělesné hmotnosti. V průběhu těhotenství se VDD pro bílkovinu zvyšuje o 15 g denně, v období plného kojení o 20 g denně. Studie s izotopy dále ukázaly, že celotělová syntéza proteinu u zdravého člověka je funkcí příjmu proteinu z potravy, kdy dosahuje svého maxima při příjmu 1,5–1,7 g proteinu/kg, den, za podmínek adekvátního příjmu energie. Vyšší příjem proteinů znamená pouze zvýšení katabolismu bílkovin s vyšším vylučováním urey (5). Při stresu u tzv. akutního pacienta nebo u pacienta v rekonvalescenci dochází ke zvýšení potřeby bílkovin téměř na dvojnásobek potřeby zdravého člověka (1,6 g/kg), přičemž vzestup spotřeby bílkovin je větší nežli zvýšení celkových energetických nároků. Z klinických a biochemických ukazatelů sníženého příjmu bílkovin je významné posouzení přítomnosti hypoalbuminemických otoků, stavu svalstva, trofických změn kůže, sledování plazmatických hladin bílkovin, zejména hodnot albuminu (těžká karence pod 28 g/l), prealbuminu (těžká karence pod 100 mg/l), transferinu (těžká karence pod 1,5 g/l), sledování bilance dusíku.
Hrazení bílkovin běžnými potravinami
Hlavními zdroji bílkovin v populacích ekonomicky vyspělých zemí jsou: maso, mléko a mléčné výrobky, vejce, ryby, luštěniny, obiloviny a zelenina včetně brambor. U smíšené stravy v rozvinutých zemích kryjí živočišné zdroje zhruba 65 % celkového příjmu bílkovin, z rostlinných zdrojů pak největší část, celkových 20 % kryjí obiloviny.
Tabulka 6: Potravinové zdroje bílkovin.
|
Zdroj
|
Zastoupení bílkovin v potravině
(váhová %)
|
Limitující AMK
|
|
Maso (svalovina s odřezaným tukem)
|
18–20
|
|
|
Mléko savců (kravské)
|
2–5 (3,5)
|
|
|
Vejce
|
13–14 (2/3 v bílku)
|
|
|
Ryby
|
10–21
|
|
|
Obiloviny
|
6–20
|
Lysin
|
|
Rýže
|
7–9
|
Lysin
|
|
Pšenice
|
12–15
|
Lysin
|
|
Luštěniny
|
20–25
|
Lysin, Methionin, Tryptofan, Threonin
|
|
Sója
|
40–42
|
|
|
Ovoce, zelenina
|
< 1
|
|
|
Brambory
|
2
|
|
|
Houby (jedlé)
|
27
|
|
|
Kvasnice (Candida utilis = torula, Saccharomyces carlsbergensis = pivovarské)
|
50 % sušiny
|
Methionin
|
|
Mořské řasy (Chlorella, Spirulina)
|
50–60 % sušiny
|
Methionin
|
Rostlinné zdroje bílkovin se liší od živočišných tím, že jsou obvykle v jedné či více esenciálních AMK limitované, tzn., že určitá esenciální AMK není přítomna vůbec nebo je její množství koncentračně velmi malé. Z tohoto důvodu je třeba, v případě hrazení bílkovin pouze rostlinnými zdroji, mít stravu pestrou a vzájemně jednotlivé zdroje kombinovat. V dětském věku jsou diety založené pouze na rostlinných zdrojích shledávány jako problémové s vysokou pravděpodobností nedostatečného hrazení některé z esenciálních AMK a vzniku dalších nutričních karencí: vitaminu B12, železa, zinku apod. Některé studie z rozvojových zemí či koncentračních táborů rovněž poukazují na zpoždění psychomotorického a mentálního vývoje dětí následkem nedostatečného přívodu esenciálních AMK. V dospělém věku pak správnou kombinací a dostatečným množstvím zdrojů rostlinného původu lze dobře zásobit lidský organismus potřebnými AMK. Navíc epidemiologické studie potvrzují v dospělém věku i některé zdravotní přednosti tohoto typu stravování, dané vyšším zastoupením rostlinných zdrojů, pestrostí stravy a pravděpodobně i celkově odlišným životním stylem vzhledem k běžné populaci.
Nedostatek příjmu bílkovin
Převážně proteinová malnutrice – kwashiorkor
Je následkem nedostatečného množství bílkovin při ještě dostačujícím krytí energetických nároků organismu. Je vyjádřena zvláště u malých dětí živených sacharidovými zdroji. Vyvíjí se během několika týdnů. Etiologickým mechanismem výsledného klinického obrazu je zachovaná produkce inzulinu vlivem dostatečného množství sacharidů, která vede k šetření svalového proteinu. To v konečném důsledku vede ke ztrátám jaterního proteinu, čímž dochází ke snížení hladiny plazmatického albuminu s následkem hypoalbuminemických edémů. Zároveň je nízká i jaterní produkce nízkodenzních lipoproteinů, která vede k hromadění lipidů v játrech a zvětšení jater. Z dalších klinických příznaků jde o pigmentaci a deskvamaci kůže, prořídnutí vlasů, celkovou apatii, nechutenství. Dítě, které je zpravidla postiženo častěji než dospělý, může mít i normální váhu vzhledem k věku. Celkově neprospívá, dochází k psychomotorické a mentální retardaci.
Proteino-energetická malnutrice – marasmus
Nastává jako důsledek hladomorů v ekonomicky neprosperujících zemích. Příčiny neschopnosti země poskytnout obyvatelstvu dostatek potravin obvykle spočívají v klimatických podmínkách, válkách, špatném ekonomickém vedení země, prudké populační explozi, katastrofách apod. Symptomy zahrnují zpomalení až zastavení růstu, hubnutí, slabost, zimomřivost, apatii, amenoreu a impotenci. Kůže je bledá, s pigmentovými skvrnami, vlasy jsou tenčí, v dospělosti často vypadávají, zornice špatně reagují na světlo. Končetiny jsou chladné, cyanotizují. Snižuje se kožní turgor, ztrácí se podkožní tuk, dochází k svalové devastaci, nehypoalbuminemickým otokům, distenzi břicha s častou přítomností krvavých průjmů. Tělesná teplota je podnormální, puls zpomalený. Psychicky jsou lidé v energetické malnutrici pasivní, depresivní, v dosahu jídla se však stávají agresivními. Stav podvýživy somatometricky charakterizuje body mass index (BMI) pod 18,5 kg/m2, obvod paže měřený v úrovni střední vzdálenosti spojnice acromion-olecranon nižší než 15,5 cm u žen a 19,5 cm u mužů, u dětí ve věku od 1 do 5 let, je-li tento obvod pod 12,5 cm.
U proteino-energetické malnutrice jsou obvykle deficitní také následující mikronutrienty: draslík, hořčík, železo, zinek, vitamin A, někdy vitamin B1, B2, kyselina listová, niacin, vitamin K, jód, esenciální MK, měď, chrom.
Adaptační změny u nekomplikovaného hladovění probíhají následovně. Během prvních 12–18 hodin dochází k vyčerpání zásob glykogenu (3780 kJ, tj. 900 kcal) z jater, svalové tkáně a myokardu. Po té nastupuje tvorba glukózy z glukogenních AMK a glycerolu. Postupně klesá sekrece inzulinu a zvyšuje se produkce kontraregulačních hormonů glukagonu, hydrokortizonu, katecholaminů. To vede ke stimulaci proteolýzy v kosterním svalstvu a viscerálních orgánech a stimulaci lipolýzy v tukové tkáni. Během týdne dochází ke snížení energetického výdeje až o 40 %, (pokles BMR, trijodtyroninu, stresových hormonů), vystupňování lipolýzy s produkcí MK do krevního oběhu, kam se také dostávají ketolátky, produkované játry. Vzestup ketogeneze zároveň chrání depleci zásob bílkovin, takže jejich katabolismus při plné adaptaci klesá ze 70 až na 20 g bílkoviny denně. Ketolátky se zároveň stávají hlavním metabolickým substrátem pro mozek. Během prostého hladovění postupně dochází k úbytku tukové tkáně a svalstva, snižuje se množství viscerálního proteinu. S prolongující se dobou hladovění se zhoršuje adaptace a člověk zpravidla po 60–70 dnech umírá. Smrt při tom nastává zpravidla v důsledku arytmie, srdečního selhání při depleci minerálů a ztrátě kritického množství bílkovin (pod 40 % celkových tělesného poolu). Při tom teprve v terminální fázi hladovění lze najít laboratorní snížení sérové hladiny prealbuminu, transferinu, albuminu, draslíku, hořčíku a fosforu.
Mezi marasmem a kwashiorkorem, dvěma hraničními stavy, je v praktickém životě vyjádřena u postižených celá řada přechodů podle vzájemného poměru nedostatku bílkoviny a energie. Intervenční přístup se skládá z úpravy dehydratace a elektrolytových poruch, ze zvládnutí acidózy, hypoglykémie, hypotermie a zaléčení infekcí. Následná realimentace se zvyšuje od hodnoty 420 kJ (100 kcal) do 630 kJ (150 kcal) a 1,5 g bílkoviny denně vztažených k 1 kg tělesné hmotnosti. Zároveň se musí doplňovat draslík, hořčík a vitaminy.
Nadbytek příjmu bílkovin
Údaje o škodlivosti nadbytečného příjmu bílkovin nejsou zcela konzistentní. Přesto zde existuje podezření na asociace mezi nadbytkem bílkovin v časném postnatálním období (porovnáno s jejich koncentrací z mateřského mléka) a dřívějším nástupem ukládání podkožního tuku na počátku školního věku, osmotickou zátěží ledvin civilizačními chorobami ve věku dospělém nadbytkem bílkovin, zejména živočišného původu a výskytem nádorových onemocnění, mechanismy: příjmu heterocyklických aminů vznikajících při tepelné úpravě bílkovin účinku produktů metabolismu nevyužitých aminokyselin (kadaverin, putrescin – podpora onkogeneze), produkcí karcinogenních N-nitrososloučenin (nitrosaminy, nitrosamidy), produkcí toxických biogenních aminů, nadbytkem bílkovin a osteoporózou, vzhledem ke zvýšenému vylučování kalcia společně s degradačními produkty bílkovin za předpokladu konstantního příjmu fosforu.
Rovněž existuje podezření mezi nadbytkem bílkovin živočišného původu a zvýšenou endogenní produkcí cholesterolu z odbourávání aminokyselin ketogenezí. Navíc zvýšený příjem tuku obvykle vázaný na příjem živočišných bílkovin vede ke zvýšení rizika kardiovaskulárních chorob.
Lipidy
Jsou organické sloučeniny, velmi málo rozpustné ve vodě. V biologických systémech mají především funkci zásobních energetických jednotek a tepelného izolátoru v podkoží, dále jsou ideální stavební součástí buněčných membrán a nervové tkáně, kdy funkcí elektrického izolátoru umožňují šíření depolarizačních vln podél myelinizovaných nervových vláken. Jsou součástí hormonů, tkáňových působků – eikosanoidů, plazmatických lipoproteinů.
Přijímané jako potraviny, vzhledem ke své dvojnásobné energetické denzitě v porovnání se sacharidy či proteiny přispívají k podstatnému zvyšování celkově přijaté energie. Navíc zvyšují chutnost potravy ovlivněním její konzistence a udržováním vůně. Ve střevě usnadňují vstřebávání vitaminů rozpustných v tucích.
Lipidy lze klasifikovat v zásadě na jednoduché lipidy (tuky = estery mastných kyselin), složené lipidy (fosfolipidy, glykolipidy, lipoproteiny…), prekurzory a odvozené lipidy (mastné kyseliny (MK), steroidy, alkoholy včetně glycerolu a sterolů, hormony…). Lipidy je možno ale také dělit na nepolární lipidy, tzv. neutrální tuky, představované zejména triacylglyceroly (TG) a polární, amfiphatické lipidy, představované zejména MK, fosfolipidy, sfingolipidy, solemi MK, v menší míře i cholesterolem. Ty se samovolně orientují na rozhraní mezi vodnou a olejovou fází, nepolárními skupinami do vodné fáze a polárními do lipidové fáze. Dvojvrstva takovýchto polárních lipidů je pokládána za základní strukturu biologických membrán.
Fyziologicky významné lipidy
Fosfolipidy
Jsou odvozeny od kyseliny fosfatidové a dělí se na fosfatidyl: -glycerol, -cholin, -ethanolamin, -serin, -inositol; lysofosfolipidy, plasmalogeny, sfingomyeliny.
Tabulka 7: Rozdělení fosfolipidů
|
Fosfolipidy:
|
Zástupce
|
Funkce v organismu
|
|
Fosfatidylglycerol
|
Kardiolipin
|
Hlavní lipid mitochondriálních membrán
|
|
Fosfatidylcholin
|
Lecithin
|
V buněčných membránách, zásoby cholinu pro přenos nervových vzruchů
|
|
Fosfatidyethanolamin
|
Kefalin
|
|
|
Fosfatidylserin,
|
|
|
|
Fosfatidylinositol
|
|
Složkou buněčné membrány, kde je prekursorem vnitřního signálu v buněčné membráně tzv. „druhého posla“ extra-intracelulární signalizace
|
|
Lysofosfolipidy
|
Lysolecithin
|
Uplatňuje se v metabolismu glycerolfosfolipidů
|
|
Plasmalogeny
|
|
V mozku a svalech
|
|
Sfingomyeliny
|
|
V mozku a nervové tkáni
|
Fosfolipidy mají nezastupitelnou strukturální úlohu jako součást buněčných (lecithin, fosfatidylinositol) a mitochondriálních (kardiolipin) membrán a nervových struktur (plasmalogeny, sfingomyeliny). Glykolipidy se dělí na glykosfingolipidy (mozek, nervová tkáň) a gangliosidy (nervová tkáň, receptorová funkce). Steroidy mají mnoho fyziologicky významných funkcí. Nejznámějším steroidem je cholesterol. Je široce rozšířen ve všech buňkách těla, zejména v nervové tkáni. Je významnou složkou buněčné membrány a lipoproteinů krevní plasmy. Ve stravě je obsažen pouze v potravinách živočišného původu. Jeho denní příjem se pohybuje kolem 300 mg denně. Existují interindividuální rozdíly ve vstřebávání cholesterolu z potravy. Nejsilnější dietní determinantou hladiny krevního cholesterolu, zejména LDL frakce, je obsah saturovaných MK, vlastní obsah cholesterolu v dietě má obvykle menší význam. Zvýšený příjem obou těchto živin snižuje LDL-receptorovou aktivitu v jaterních buňkách a tak zvyšuje plazmatickou hladinu LDL cholesterolu. Od cholesterolu jsou odvozeny ostatní steroidy, mezi které patří: hormony kůry nadledvin, pohlavní hormony, vitamin D, srdeční glykosidy, žlučové kyseliny.
Triacylglyceroly (triglyceridy – TG)
Jsou esterově vázané MK na glycerol. U obratlovců a tedy i u člověka jsou uskladněny ve specifických buňkách – adipocytech, kdy TG kapénky vyplňují téměř celou buňku. Protože na sebe neváží vodu, představují v malém objemu ideální zásobní metabolické palivo pro většinu eukaryotických buněk. Subkutánní adipocytární tkáň navíc slouží k tepelné izolaci organismu. V rostlinách jsou TG obsaženy v semenech rovněž jako zásobní zdroj energie pro potřeby klíčení.
V potravě člověka představují TG hlavní součást přijímaných tuků. Rostlinné oleje, mléčné produkty a živočišný tuk jsou směsicí jednoduchých a smíšených TG. Trávením a hydrolýzou se z nich uvolňují volné MK, monoglyceridy a menší množství monoacylfosfolipidů. MK jsou vysoce redukované hydrouhličité deriváty, jejichž oxidace v buňkách je vysoce exotermní. Nejběžněji se vyskytují MK s 12–24 uhlíky seřazenými v lineárním řetězci. MK se dále dělí podle počtu dvojných vazeb na nasycené (saturované, SMK), které neobsahují dvojnou vazbu ve svém řetězci, na monoenové MK (MMK) s jednou dvojnou vazbou a MK polyenové (PMK) s více dvojnými vazbami, z nichž se podle umístění první dvojné vazby od metylového konce rozlišují fyziologicky významné řady MK n-6 (ω-6) a n-3 (ω-3). Podle počtu atomů uhlíku se dále vyčleňují MK s krátkým řetězcem, které obsahují méně než 6 atomů uhlíku a MK s dlouhým řetězcem od 7 do 22 uhlíků. Délka řetězce a zastoupení nenasycených vazeb v MK obsažených v TG rozhoduje o fyzikálních vlastnostech TG. Proto jsou při pokojové teplotě rostlinné oleje složené z TG obsahujících nenasycené MK tekuté a živočišné tuky obsahující převážně SMK tuhé. Tuky jsou náchylné při dlouhodobé expozici vzdušnému kyslíku ke žluknutí, kdy oxidací nenasycených vazeb vznikají aldehydy a těkavé MK s krátkým řetězcem. Žluklé tuky nejsou poživatelné.
Tabulka 8: Zastoupení MK ve 100 g zdrojového potravinového tuku. Volně zadaptováno podle zdrojů (6,7,8).
|
Mastné kyseliny (MK)
|
SMK
|
MMK
|
PMK
|
|
|
Zastoupení MK v gramech ve 100 g zdrojového tuku.
|
Nasycené
o 4-12 C
|
Myristová
|
Palmitová
|
Stearová
|
Palmitoolejová
|
Olejová
|
Linolová
|
Linolenová
|
Ikosenová,
dokosenová
|
Arachidonová
|
|
|
|
4-12:0
|
14:0
|
16:0
|
18:0
|
16:1
|
18:1
|
18:2
|
18:3
|
20:122:1
|
20:4
|
Suma
PUFA
|
další
|
|
Hovězí (sval)
|
|
|
16
|
11
|
2
|
20
|
26
|
1
|
|
13
|
|
11
|
|
Jehněčí (sval)
|
|
|
22
|
13
|
2
|
30
|
18
|
4
|
|
7
|
|
4
|
|
Jehněčí (mozek)
|
|
|
22
|
18
|
1
|
28
|
1
|
|
|
4
|
14
|
12
|
|
Kuře (sval)
|
|
|
23
|
12
|
6
|
33
|
18
|
1
|
|
6
|
|
1
|
|
Kuře (játra)
|
|
|
25
|
17
|
3
|
26
|
15
|
1
|
|
6
|
6
|
1
|
|
Vepřové (sval)
|
|
|
19
|
12
|
2
|
19
|
26
|
|
|
8
|
|
14
|
|
Treska (maso)
|
|
|
22
|
4
|
2
|
11
|
1
|
|
|
4
|
52
|
4
|
|
Listová zelenina
|
|
|
13
|
S
|
3
|
7
|
16
|
56
|
|
|
|
5
|
|
Sádlo I
|
|
1
|
29
|
15
|
3
|
43
|
9
|
1
|
|
|
|
|
|
Sádlo II
|
|
1
|
21
|
12
|
3
|
46
|
16
|
1
|
|
|
|
1
|
|
Drůbeží tuk
|
|
1
|
27
|
7
|
9
|
45
|
11
|
1
|
|
|
|
1
|
|
Hovězí lůj
|
|
3
|
26
|
8
|
9
|
45
|
2
|
2
|
|
|
|
7
|
|
Skopový lůj
|
|
3
|
21
|
20
|
4
|
41
|
5
|
1
|
|
1
|
|
6
|
|
Mléko kravské
|
13
|
12
|
26
|
11
|
3
|
29
|
2
|
1
|
|
|
|
4
|
|
Mléko kozí
|
21
|
11
|
27
|
10
|
3
|
26
|
2
|
|
|
|
|
|
|
Žloutek
|
|
|
29
|
9
|
4
|
43
|
11
|
|
|
|
|
4
|
|
Olej z tresčích jater
|
|
|
13
|
3
|
13
|
20
|
2
|
|
18
|
|
20
|
5
|
|
Avokádo
|
|
|
20
|
1
|
6
|
60
|
18
|
|
|
|
|
1
|
|
Kokos
|
63
|
16
|
9
|
2
|
|
7
|
2
|
|
|
|
|
1
|
|
Kukuřice
|
|
1
|
14
|
2
|
|
30
|
50
|
2
|
|
|
|
1
|
|
Oliva
|
|
|
12
|
2
|
3
|
72
|
11
|
1
|
|
|
|
2
|
|
Palma
|
|
1
|
42
|
4
|
|
43
|
8
|
S
|
|
|
|
2
|
|
Palma – jádro
|
53
|
18
|
9
|
3
|
|
15
|
2
|
|
|
|
|
|
|
Burský ořech
|
|
1
|
11
|
3
|
|
49
|
29
|
1
|
|
2
|
|
6
|
|
Řepka (vysoce eruková)
|
|
|
4
|
1
|
2
|
24
|
16
|
11
|
43
|
2
|
|
1
|
|
Řepka (nízko eruková)
|
|
|
4
|
1
|
|
54
|
23
|
10
|
|
|
|
8
|
|
Saflor (vysoce olejová)
|
|
|
5
|
2
|
|
73
|
17
|
1
|
|
|
|
2
|
|
Saflor (vysoce linolová)
|
|
|
6
|
3
|
|
15
|
73
|
1
|
|
|
|
2
|
|
Sója
|
|
|
10
|
4
|
|
25
|
52
|
7
|
|
|
|
2
|
|
Slunečnice
|
|
|
6
|
6
|
|
33
|
52
|
S
|
|
|
|
3
|
|
4-12:0
|
14:0
|
16:0
|
18:0
|
16:1
|
18:1
|
18:2
|
18:3
|
20:122:1
|
20:4
|
Suma
PUFA
|
další
|
|
Zastoupení MK v gramech ve 100 g zdrojového tuku.
|
Nasycené
o 4-12 C
|
Myristová
|
Palmitová
|
Stearová
|
Palmitoolejová
|
Olejová
|
Linolová
|
Linolenová
|
Ikosenová,
dokosenová
|
Arachidonová
|
|
|
|
Mastné kyseliny (MK)
|
SMK
|
MMK
|
PMK
|
|
SMK a MMK mohou být syntetizovány z acetyl koenzymu A a nejsou proto ve výživě nezbytné. Esenciální je naopak malé množství PMK, které jsou důležitými prekurzory fosfolipidů v buněčných membránách a ikosanoidů, odvozených od arachidonové kyseliny. Esenciální MK jsou: kyselina linolová (C18:2; n-6) a kyselina alfa-linolenová (C18:3; n-3). Z nich v těle vytvářené kyseliny: arachidonová (C20:4; n-6), kyselina eikosapentaenová EPA (C20:5; n-3) a dokosahexaenová DHA (C22:6; n-3), které se při omezeném příjmu jejich prekurzorů ve stravě stávají esenciálními rovněž. Při nedostatku esenciálních MK dochází ke změnám ve složení lipidů v mnoha tkáních (zvláště v buněčných membránách). Zároveň se snižuje účinnost oxidace MK v mitochondriích. Nedostatek kyseliny linolové ve výživě člověka (pod 1–2 % celkově přijaté energie, tj. při menším příjmu než 2–5 g denně) se projevuje suchostí kůže, ztrátou vlasů, zhoršeným hojením ran (pacienti s biliární atresií, cystickou fibrózou, při parenterální bezlipidové dietě). V experimentu na krysách byla navíc zjištěna porucha růstu, reprodukce, degenerace a zhoršená funkce mnoha dalších orgánů. Esenciální MK tvoří až 50 % suché váhy mozku. Jejich vysoké zastoupení v mateřském mléce svědčí o jejich důležité roli ve výživě u rychle se vyvíjejícího mozku v raném dětském věku.
Na regulačních funkcích organismu se podílejí tzv. „eikosanoidy“, tkáňové působky, odvozené od dvacetiuhlíkových nenasycených MK, zejména kyseliny arachidonové. V zásadě se dělí na prostaglandiny, leukotrieny a tromboxany. Prostaglandiny zprostředkovávají buněčné a tkáňové funkce řízené přes regulaci syntézy intracelulárního c-AMP, stimulují tak např. kontrakci hladkého svalstva, krevní průtok specifickými orgány, cyklus bdění-spánku, odpověď tkání na adrenalin, glukagon, zprostředkovávají zvýšení tělesné teploty, zánět, bolest. Leukotrieny se podílejí na kontrakci hladké svaloviny dýchacího traktu při anafylaktické odpovědi. Tromboxany modulují krevní srážlivost, krevní průtok. Rostou důkazy o tom, že nutriční stav s ohledem na vzájemný poměr PMK řady n-6 a n-3 alteruje produkci eikosanoidů s ovlivněním destičkových funkcí, vazomotoriky cévní stěny a zánětlivých odpovědí.
Při příjmu vysokého množství PMK hrozí nebezpečí peroxidace (autooxidace) lipidů vystavených kyslíku. Jde o řetězovou reakci, poskytující neustálý přísun volných radikálů, které jsou podezřelé z poškozování tkání ve smyslu iniciace rakoviny, zánětlivých onemocnění, aterosklerózy, stárnutí. Procesu peroxidace až už ve fázi iniciace či během peroxidace brání antioxidanty. V potravinách jde zejména o vitamin E, který je rozpustný v tucích a také je obvykle obsažen v přírodních zdrojích mastných kyselin. Z dalších antioxidačních přirozených látek je významná kyselina močová (urát), vitamin C, při nízkém pO2 může působit jako antioxidant i beta karoten. Z aditiv se cíleně jako antioxidantů používá propylgallát, butylovaný hydroxyanisol a butylovaný hydroxytoluen. In vivo pak působí superoxiddismutáza, uráty, vitamin E. Proto se zvyšují požadavky na antioxidační látky, především vitamin E. Z těchto důvodů ale i na základě ještě nedostatečného množství informací o účincích dlouhodobě vysokého příjmu PMK se nedoporučuje jejich zastoupení ve stravě vyšší než 10 % celkové denní energie. VDD pro dospělé doporučuje 2–3 g kyseliny linolové za den, což odpovídá 1-2 % celkové denní energie. U dětí pak 0,2 g/kg (tj. 2,7 % celkové denní energie).
Tabulka 9: Převzato podle (9).
|
Ryby
|
Celkový obsah EPA a DHA g/100 g zdroje
|
|
Makrela (z Atlantiku)
|
2,5
|
|
Losos (z Atlantiku)
|
1,8
|
|
Sleď (z Pacifiku)
|
1,7
|
|
Sleď (z Atlantiku)
|
1,6
|
|
Pstruh jezerní
|
1,6
|
|
Tuňák
|
1,6
|
|
Jeseter
|
1,5
|
|
Sardel (ančovička)
|
1,4
|
|
Šprot
|
1,3
|
|
Sardinka
|
1,1
|
Dietní zdroje a obvyklý příjem
Většina snědeného tuku je představována TG. Průměrný dospělý jich zkonzumuje denně kolem 70–140 gramů, zatímco např. cholesterolu z potravy se sní kolem 300 miligramů. Více než polovina veškerého přijatého tuku je přijata formou živočišných potravin: separovaný živočišný tuk (sádlo, máslo), červené maso (vepřové, hovězí, uzeniny), drůbeží, rybí maso, mléko a mléčné produkty, vejce. Největším zdrojem nenasycených mastných kyselin pak jsou oleje (rostlinné, rybí), majonézy, dresinky. Také sója, ořechy, mák a další olejnatá semena obsahují tuk.
Živočišný tuk obsahuje vyšší zastoupení SMK a MMK. Proměnlivost zastoupení jednotlivých MK v tukové tkáni živočichů závisí na živočišném druhu, je však ovlivněna i jeho krmivem. Např. krmení skotu drcenými olejnatými semeny či ovsem zvyšuje zastoupení nenasycených MK v jejich mléce.
Svalovina libového masa obsahuje tuk ve formě fosfolipidů a volného cholesterolu. Z MK se jedná z 85 % o kyselinu palmitovou, stearovou, olejovou, linolovou, arachidonovou.
Ryby můžeme podle obsahu tuku dělit na netučné, typu tresky, které mají svou rezervu tuku v játrech, a ryby tučné, typu makrely a sledě, uskladňující tuk v mase. Oleje z obou druhů ryb obsahují hodně 20 a více uhlíkatých PMK s 5 či 6 dvojnými vazbami opět v závislosti na druhu, krmivu a ročním období.
Mléko a mléčný tuk v něm obsažený je složen z TG, fosfolipidů a cholesterolu. Z MK převažují kyseliny s krátkým až středně dlouhým řetězcem.
Jedno vejce obsahuje 6–7 g TG a fosfolipidů a 250–300 mg cholesterolu.
Olejnatá semena uskladňují TG většinou v endospermu (sója, řepka, slunečnice, palma), dužnaté ovoce typu avokáda v exokarpu. Kokosový a palmový tuk obsahuje na rostliny neobvykle vysoké zastoupení SMK. Olejnatá semena dále obsahují fosfolipidy, chlorofyly, karotenoidy, tokoferoly, rostlinné steroly a některé neobvyklé MK, jako např. erukovou MK, která může být ve velkém množství pro člověka toxická.
Listnatá zelenina jako je salát, zelí, kapusta, či zeleně zbarvená zelenina obsahuje z hlediska lidské výživy významné množství alfa-linolenové MK.
MK jsou využívány jako zdroj energie většinou buněk člověka s výjimkou erytrocytů a nervových buněk, které využívají pouze glukózu, ev. ketolátek v případě nouze. Nadbytek přijaté energie z potravy je ukládán opět ve formě TG uvnitř adipocytů tukové tkáně.
V rozvinutých zemích, zejména ve vyšších socioekonomických vrstvách, dochází v posledních letech ke změně trendu konzumace tučných výrobků ve smyslu snížení jejich konzumace upřednostňováním nízkotučných výrobků a náhradou červeného masa drůbežím a rybím.
Vzhledem k riziku kardiovaskulárních chorob a některých nádorových onemocnění (karcinom prsu, kolorektální karcinom) spojených s nadbytkem tuků ve výživě byla přijata pro zdravou dospělou populaci následující doporučení:
- snížení celkové konzumace tuku na maximálně 30 % celkového energetického příjmu
- SMK by se měly podílet 8–10 %, MMK 10–12 %, PMK do 10 % na celkovém energetickém příjmu, přičemž vzhledem k současným zvyklostem by se měl zvýšit podíl PMK z rybího tuku a podíl antioxidačních faktorů ze stravy (zejména vitamin E)
- cholesterol ze stravy by měl být nižší než 300 mg/den.
Tabulka 10: Zjednodušené schéma klasifikace, zdrojů a potřeb MK
|
Klasifikace MK:
|
Potravinové zdroje
|
Potřeba v % celkové přijaté energie
|
|
SMK
|
Živočišné tuky (kokos, palma)
|
8–10
|
|
MMK
|
Olivový, řepkový, saflorový olej, avokádo, ořechy,
|
10–12
|
|
PMK
|
n-3
|
Rybí tuk
|
Do 10
|
|
n-6
|
Rostlinné oleje (s výjimkou zdrojů MMK)
|
Sacharidy
Jsou důležitou součástí stravy. Chemicky jde o polyhydroxyaldehydy a polyhydroxyketony. Podle počtu atomů uhlíků se rozeznávají triózy, tetrózy, pentózy, hexózy atd. Podle počtu cukerných jednotek vázaných v molekule se sacharidy dělí na monosacharidy (jedna cukerná jednotka), oligosacharidy (2–10 cukerných jednotek spojených glykosidovými vazbami), polysacharidy (glykany, více než 10 cukerných jednotek) a složené – komplexní sacharidy, které obsahují i jiné sloučeniny, jako např. peptidy, proteiny a lipidy. Sacharidy vznikají v přírodě v buňkách fotoautotrofních organismů asimilací vzdušného oxidu uhličitého v přítomnosti vody při využití energie denního světla tzv. fotosyntézou. Jejich zdroji v potravě jsou kromě mléka potraviny rostlinného původu. Jsou levné a relativně celosvětově dostupné.
Tabulka 11: Klasifikace a potravinové zdroje sacharidů. (PS = polysacharidy)
|
Jednoduché sacharidy
|
Polysacharidy (PS)
|
Dělení
|
|
Monosacharidy
|
Disacharidy
|
Stravitelné PS
|
Nestravitelné PS (Vláknina potravy)
|
|
Glukóza, Fruktóza, Mannóza, Galaktóza
|
Maltóza
|
Sacharóza
|
Laktóza
|
Škrobové PS s výjimkou rezistentních
|
Rezistentní škroby
Neškrobové PS
|
Zástupci
|
|
Med, ovoce, džus
|
Klíčky obilovin a sladu
|
Řepný cukr, javorový sirup
|
Mléko
|
Obiloviny
Luštěniny
Brambory
|
Zelenina
Ovoce
Luštěniny
|
Potravinové zdroje
|
|
Glukóza, Fruktóza, Galaktóza
|
Glukóza
|
Glukóza, Fruktóza
|
Glukóza Galaktóza
|
Glukóza
|
Acetát, Propionát Butyrát
|
V tenkém střevě
|
Volná D-glukóza (synonyma: dextróza, hroznový či škrobový cukr) společně s D-fruktózou (levulóza, ovocný cukr) jsou hlavními monosacharidy většiny potravin. V relativně velkém množství jsou zastoupeny v ovoci, kde jejich obsah značně kolísá v závislosti na druhu ovoce, stupni zralosti, podmínkách posklizňového skladování a zpracování. Dále jsou monosacharidy obsaženy v medu, ve vínech, zelenině, luštěninách, vaječném bílku. Glukóza i fruktóza jsou kariogenními (kaz vyvolávajícími) cukry. V malém množství je v potravinách ještě jako monosacharid přítomna D-mannóza a D-galaktóza. Z pentóz pak D-ribóza, D-xylóza a L-arabinóza. D-ribóza je fyziologicky významným monosacharidem lidského těla, protože je součástí nukleových kyselin, koenzymů, flavoproteinů. D-xylóza se vyskytuje v gumách z dřevin, proteoglykanech, glykosaminoglykanech. L-arabinóza je složkou glykoproteinů a nachází se v arabské gemě, gumách ze švestek a třešní. Nejvýznamnějšími mezi oligosacharidy jsou sacharóza (řepný a třtinový cukr), laktóza (mléčný cukr) a maltóza (vznikající štěpením škrobu v obilovinách). Monosacharidy a disacharidy se označují také jako jednoduché sacharidy.
Polysacharidy z potravy se podle schopnosti být štěpeny lidskými sacharidázami dělí na tzv. stravitelné (využitelné) polysacharidy, kam patří většina polysacharidů škrobové povahy a tzv. nestravitelné polysacharidy, označované jako vláknina potravy. Stravitelné jsou při trávení v lidském organismu štěpeny na oligosacharidy a monosacharidy a využívány jako zdroj energie.
Vláknina
Část škrobových polysacharidů, označovaná jako rezistentní škroby, je společně s neškrobovými polysacharidy rezistentní k hydrolýze trávicími šťávami člověka. Tyto nestravitelné (nevyužitelné) polysacharidy, společně s ligninem, látkou nesacharidové povahy, jsou souhrnně označovány jako vláknina potravy a jsou definovány jako „všechny tzv. nevyužitelné polysacharidy, včetně polysacharidů, využívaných jako potravinářská aditiva“. Procházejí v nezměněné formě tenkým střevem a mohou být fermentovány teprve účinkem enzymů mikroflóry tlustého střeva za vzniku využitelných MK s nízkým počtem uhlíků (kyselina octová, propionová, máselná). Konečnými produkty fermentace vlákniny jsou dále plyny: oxid uhličitý, vodík, methan. Mezi neškrobové polysacharidy patří celulóza, hemicelulózy, pektin, inulin.
Hlavními potravinovými zdroji stravitelných, škrobových polysacharidů jsou škroby (α-glukosidový polymer, sestávající ze dvou složek amylózy a amylopektinu). Nachází se zejména v obilovinách a jejich produktech (pšeničná mouka, chléb, rýže, kukuřice, oves), bramborech, luštěninách a zelenině. Škrobový polysacharid živočišného původu – glykogen má ve výživě člověka minimální význam, protože se po smrti živočichů rozkládá.
Nestravitelné polysacharidy jsou obsaženy v zelenině, luštěninách, ovoci, obilovinách. Obsah rezistentních škrobů závisí na druhu potravin, zvyšuje se technologickými procesy výroby potravin jako je lyofilizace, nebo dlouhé ochlazování vařených potravin. Celulóza je nejrozšířenější organická molekula v přírodě. Je součástí rostlinného pletiva. Je značně rezistentní i vůči mikrobiální hydrolýze. Hemicelulózy jsou rezistentní méně. Pektin je převládajícím polysacharidem v ovoci. V cibuli, česneku, topinamburech, černém kořenu, artyčocích, čekance se vyskytuje inulin, zařazovaný mezi fruktooligosacharidy. Lignin, nesacharidová dřevnatá komponenta vlákniny stravy, se nachází v otrubách, poživatelných semenech ovoce (rybíz, jahody) a lidským organismem prochází intaktní. Polysacharidy rostlinných gum a slizů, mořských řas, mikroorganismů a modifikované škroby a celulózy se používají jako potravinářská aditiva a slouží jako plnidla, zahušťovadla a disperzní stabilizátory. Z nich celosvětově nejpoužívanější jsou guarová a lokustová guma, karagenany, agary, arabská guma, pektiny, algináty, karboxymethylcelulóza jako modifikovaná celulóza a xanthany.
Tabulka 12. Vláknina potravy
|
Polymery:
|
|
Rezistentní škrobové polysacharidy
|
glukózy
|
|
Celulóza
|
glukopyranózy
|
|
Hemicelulózy
|
heterogenní
|
|
Pektin
|
rhamno-, gluko- galaktopyranózy
|
|
Inulin
|
fruktofuranózy
|
|
Polysacharidy mořských řas a mikroorganismů (algináty)
|
manno-, galakto- a gulopyranózy
|
|
Rostlinné gumy (arabská, ghatti, karaja, modřínová)
|
galaktopyranózy, glukomannanů, galaktomannanů
|
|
Rostlinné slizy (okra)
|
rhamno-, galaktopyranózy
|
|
Modifikované polysacharidy
|
Glukopyranózy
|
|
Fruktooligosacharidy
|
Fruktózy
|
|
Lignin
|
Fenylpropanu
|
Odhaduje se, že asi 75 % příjmu energie zajišťované sacharidy poskytují stravitelné polysacharidy a 25 % oligosacharidy, mono- a disacharidy.
Po přijetí sacharidů potravou dochází vlivem sacharidáz ke štěpení stravitelných škrobových polysacharidů i disacharidů na monosacharidy. Glukóza, nejdůležitější monosacharid, je základním energetickým substrátem metabolismu prakticky každé buňky lidského organismu. Její aerobní oxidací vznikají v konečné fázi oxid uhličitý, voda a energie (38 molekul ATP z 1 molekuly glukózy). Při anaerobní glykolýze vznikají z jedné molekuly glukózy dvě molekuly kyseliny mléčné nebo ve svalu také alaninu a dvě molekuly ATP. Glukóza je nepostradatelná pro některé tkáně, které nejsou schopny normální oxidace v mitochondriích. Jde především o červené a bílé krvinky, dřeň ledvin. Také pro centrální nervový systém představuje glukóza výhradní zdroj energie, zastupitelný pouze ketolátkami v případě hladovění. Neglukózové monosacharidy jako je fruktóza, galaktóza jsou metabolizovány v játrech, kde často slouží jako substrát pro glukózu. Hlavní metabolickou cestou syntézy glukózy v organismu je ale proces glukoneogeneze z glukogenních aminokyselin a glycerolu, ev. Coriho cyklus z laktátu využitím energie vzniklé při oxidaci MK. Glukoneogeneze probíhá hlavně v játrech a částečně v ledvinách. Je stimulována glukagonem, glukokortikoidy a inhibována inzulinem. Dostatečný příjem sacharidů potravou zabraňuje u zdravého organismu odbourávání endogenního proteinu a urychlené oxidaci tuků s následnou acidózou. Zásoby sacharidů ve formě glykogenu, uskladněného v játrech, svalové tkáni a myokardu, jsou malé. Slouží pouze akutní potřebě glukózy, ev. energie a vystačí zhruba na 12–18 hodin. Glykogen není jako energetická zásoba nejefektivnější, protože váže vodu a zaujímá tak v porovnání s tuky na jednotku energie velký objem.
Příjem nestravitelných polysacharidů potravou má v lidském organismu zcela jiný význam. Podle účinku dělíme vlákninu stravy na rozpustnou (pektin, inulin, některé hemicelulózy, rostlinné slizy, gumy, rezistentní škroby, fruktooligosacharidy; v ovoci, ovsu, sladu, luštěninách, bramborech) a nerozpustnou (lignin, celulóza, některé hemicelulózy; v zelenině, otrubách a celozrnných výrobcích). Rozpustná vláknina zpomaluje rychlost pasáže gastrointestinálním traktem, v tenkém střevě omezuje absorpci některých živin a zpomaluje rychlost resorpce glukózy, čímž se snižuje strmost vzestupu glykémie. Má rovněž hypocholesterolemický účinek. Nerozpustná vláknina zvyšuje objem stolice, tím zřeďuje koncentraci toxických látek, zkracuje tranzitní čas stolice tlustým střevem. Tak omezuje kontakt a zároveň i vstřebávání toxických látek buňkami tlustého střeva. Má do jisté míry i hrubou mechanickou čistící funkci ve střevě.
Fermentací vlákniny vznikají MK s krátkým řetězcem (acetát, propionát, butyrát). Jsou významným energetickým lokálně dostupným a působícím substrátem pro buňky sliznice tlustého střeva. Podle převládajícího místa fermentace poskytují pektin, rostlinné slizy, gumy výživu buněk proximální části tlustého střeva, zatímco rezistentní škroby, fruktooligosacharidy, výživu v distální části. Řada studií navíc potvrzuje významný protinádorový účinek butyrátu. Některé z vláknin působí i jako prebiotika, (např. fruktooligosacharidy) podporou růstu lidskému organismu prospěšných bifidobakterií, produkujících látky s antibiotickými a imunomodulačními účinky, které brání růstu nežádoucí mikroflóry (Escherichia Coli, Proteus, Staphylococcus Aureus, Salmonella Typhosa), která se může podílet na vzniku toxických produktů fermentace jako je amoniak, aminy, nitrosaminy, fenoly, indoly a další. Bifidobakterie také přispívají k výživě hostitelského organismu produkcí vitaminů skupiny B. Vláknina souhrnem svých fyziologických účinků ve střevě snižuje riziko vzniku kolorektálního karcinomu. Uplatňuje se v léčbě divertikulózy, zácpy.
Doporučená dávka stravitelných sacharidů v potravě je 55–60 % CEP, tj. kolem 270–350 event. více gramů denně v závislosti na celkové dávce energie. Na 1 g bílkoviny a 1 gram tuků by tak měly připadat ve výživě dospělého člověka 4 gramy sacharidů. Polysacharidy mají tvořit většinu sacharidů, neboť nadbytek jednoduchých cukrů je spojován se zvýšením rizika zubního kazu, náchylností k obezitě a při nadměrném příjmu sacharózy (řepného cukru) i možného vzniku mikronutrientních karencí vzhledem k přijímané dávce energie. Denní příjem vlákniny by měl u dospělého člověka představovat 25–35 gramů.
Mikronutrienty ve výživě
V současné době jsou mimo klasicky známé karenční stavy z mikronutrientních deficitů rozpoznávány kromě jejich kofaktorových funkcí také funkce biologických regulátorů a modulátorů. Mohou tak ovlivnit genovou expresi, maximalizovat fyziologickou funkci, oddalovat či předcházet chronickým nemocem atd.
Tabulka 13: Základní funkce mikronutrientů
|
Krebsův cyklus (intermediární metabolismus)
|
Vitaminy:
B1, B2, B6, niacin, biotin, B12, C, E, pantothenová a listová kyselina
Minerály:
Mg, K, Mn, Ca, Zn, Cu, Co, S, Cr, Fe, Se
|
|
Antioxidanty (v koncentracích obsažených v běžné stravě se chovají jako antioxidanty a mají protektivní účinky, jsou-li podávány ve vysokých dávkách jako suplementa, mohou se za určitých podmínek chovat naopak prooxidačně a organismus poškozovat, jak to dokládají studie s podáváním beta karotenu u kuřáků).
|
Vitaminy:
A, karotenoidy – beta karoten, C, E
Minerály:
Mn, Zn, Cu, Co, S, Cr, Se
|
|
Kognitivní funkce
|
Vitaminy:
B1 (beri-beri, Wernicke-Korsakovova psychóza),
B6 (periferní neuropatie, křeče),
Niacin (demence při pelagře),
B12 (periferní neuropatie, subakutní kombinovaná systémová degenerace, demence)
pantothenová kyselina (myelinová degenerace)
listová kyselina (iritovanost, deprese? Paranoia?)
E (spinocerebelární degenerace, periferní axonopatie)
Fe, B12 a listová kyselina (anémie)
Minerály: J (hypotyreóza, kretenismus)
|
|
Imunita a integrita kůže a sliznic
|
Vitaminy:
A, C, E, B6, B12 a listová kyselina
Minerály:
Cu, Fe, Mn, Zn
|
|
Kosti a (kolagen)
|
Vitaminy:
D, (C), (K)
Minerály:
Ca, P, Mg, Mn, B, F, (Cu, Zn, Fe)
|
|
Buněčná signalizace
|
Ca
|
Vitaminy rozpustné ve vodě
Tabulka 14: Vitamíny rozpustné ve vodě a jejich funkce
flavin adenosin dinukleotid (FAD), nikotinamid adenosin dinukleotid (NAD) a jeho fosfát (NADP)
|
Průměrná denní potřeba dospělým
|
Funkce
|
Projevy nedostatku
|
Potravinové zdroje
|
|
B1 (thiamin)
1,5–2,0 mg
závisí na výdeji energie a příjmu sacharidů
|
Enzymatické dekarboxylace alfa ketokyselin, kofaktor transketolázy, nutný pro intermediální metabolismus.
|
„Beri-beri“ v „mokré formě“ s kardiálními příznaky a „suché formě“ s neurologickými projevy.
Wernicke-Korsakovův syndrom = encefalopatie, poruchy koordinace a zmatenost.
|
Kvasnice, povrchové vrstvy obilovin, luštěniny, méně v mléce, mase, zelenině.
Ničí se alkalickým prostředím či teplotami nad 100 0C.
|
|
B2 (riboflavin)
1,5–2,0 mg
|
Oxidačně-redukční reakce jako součást flavoproteinových enzymů (FAD, NAD), nutný pro intermediální metabolismus.
|
Postižení kůže a sliznic (ragády ústních koutků), neuropatie s parestéziemi dolních končetin a ataxie, anémie, zpomalení vývoje intelektu u dětí, pokles duševní výkonnosti u dospělých, poruchy imunity.
|
Kvasnice, játra, povrchová vrstva obilovin, mléko, maso.
Rozkládá se vlivem denního světla.
|
|
Niacin (B3, PP, kys.
nikotinová)
16–22 mg
|
Podílí se na oxidativní fosforylaci jako součást NAD, NADP.
|
Pelagra: diarea, demence a dermatitida (zarudlá, hrubá kůže s puchýři a hnědou pigmentací na osvětlené části těla).
|
Kvasnice, otruby, tmavý chléb, maso (málo v kukuřici).
Provitamínem je tryptofan.
|
|
B6 (pyridoxamin, pyridoxol a pyridoxal)
1,4–2,0 mg; 15–20 µg/g bílkoviny
|
V enzymech katalyzujících transaminace, racemizace a dekarboxylace AMK.
|
Seborrhoická dermatitida v obličeji, záněty rtů, jazyka dutiny ústní, hypochromní anémie, periferní neuritidy, předrážděnost a zpomalení psychomotorického vývoje u dětí.
|
Kvasnice, pšeničné klíčky, sója, játra, vnitřnosti, maso.
|
|
Pantothenová kys.
8–10 mg
|
Součástí koenzymu A, nosiče acylových skupin = nutná pro intermediární metabolismus a všechny základní živiny.
|
Nedostatek je vzácný s projevy: myelinová degenerace, anémie, únavnost, typické pálení chodidel vypadávání vlasů, ztráta pigmentace.
|
Játra, kvasnice, žloutek, maso, mléko, sója, mouka.
Ničí se v silně kyselém či zásaditém prostředí, vlivem kyslíku a ultrafialových paprsků, rozmrazováním potravin). Produkován střevní flórou.
|
|
Biotin (H)
30–200 µg
|
Koenzym karboxyláz včetně acetyl-CoA karboxylázy a pyruvátkarboxylázy (intermediární metabolismus, syntéza lipidů, glukoneogeneze).
|
Hypercholesterolémie, porucha glukózové tolerance.
Vypadávání vlasů, zažívací a neurologické poruchy při parenterální výživě.
|
Mateří kašička, kvasnice, čokoláda, květák, hrášek houby, játra, maso, tuky, vnitřnosti, ryby, žloutek.
Odolný vůči zevním vlivům. Tvořen střevní flórou. Antivitaminem je avidin.
|
|
Listová kys. (N, folacin)
200–400 µg
|
Přenašeč jednouhlíkatých skupin (nutná pro dělící se buňky – syntéza nukleových kyselin, metabolismus homocysteinu)
|
Hyperhomocysteinemie a riziko aterosklerózy. Útlum krvetvorby, porucha růstu, celková slabost, záněty v dutině ústní. Rozštěp neurální trubice v graviditě.
|
Listová zelenina, ořechy, luštěniny, obiloviny, játra, vnitřnosti, žloutek, mléko. Citlivá na teplo, světlo (sušení), kyseliny, zásady.
|
Tabulka 15: Vitamíny rozpustné ve vodě a jejich funkce
|
Průměrná denní potřeba dospělým
|
Funkce
|
Projevy nedostatku
|
Potravinové zdroje
|
|
B12
|
V transmetylačních enzymech, syntéza hemu, AMK, nukleových kyselin, metabolismus MK. Slouží také k recyklaci folátových koenzymů
|
Makrocytární anémie, demyelinizace neuronů s postižením zadních provazců míšních a poruchou kognitivních funkcí. Hyperhomocysteinemie a riziko aterosklerózy.
|
Živočišné zdroje, zejména játra; zčásti je syntetizován střevními bakteriemi. Pro vstřebání v ileu nezbytný vnitřní faktor.
|
|
C (kys. askorbová a hydroaskorbová)
30–200 mg
|
Tvoří oxido-redukční systém s funkcí donoru elektronů.
Kofaktor hydroxylačních reakcí (syntéza kolagenu, katecholaminů, karnitinu).
Antioxidant (obnovuje aktivní formu E vitamínu)
Přeměna cholesterolu na žlučové kyseliny.
Zvyšuje resorpci železa.
Detoxikace cizorodých látek
Brání tvorbě karcinogenních nitrosaminů.
Ovlivňuje permeabilitu buněčných membrán.
|
Těžká karence = skorbut (krvácení z dásní, pod kůži, do svalů, vnitřních orgánů, krvácením u dětí do periostu dlouhých kostí, vypadávání zubů. Terminálními symptomy jsou ikterus, edémy, teploty, křeče, šok, náhlá smrt.
Epidemiologická data svědčí ve prospěch ochranného účinku stravy bohaté kyselinou askorbovou v prevenci kardiovaskulárních nemocí, katarakty a některých nádorů (karcinomu žaludku, jazyka, hltanu, jícnu, hrtanu, plic, pankreatu, děložního hrdla, prsu).
|
Čerstvé ovoce (jahody, citrusy, černý rybíz) a zelenina (zejména zelené části rostlin, brambory), játra.
Snadno se ničí nesprávným zpracováním (oxidace kovy), sušením, zahříváním v neutrálním a alkalickém prostředí.
Jeho maximální tělesné zásoby představují 5 g s 3 % denním obratem.
|
Tabulka 16: Hydrosolubilní vitaminy, laboratorní potvrzení deficitu
|
Deficit
|
Rizikové skupiny
|
|
B1
|
Vysoká aktivita erytrocytární transketolázy
u. thiamin/kreatinin < 5 µmol/mmol
|
Alkoholici, realimentovaní jedinci po hladovění, jedinci na sacharidové stravě, hemodialyzovaní pacienti.
|
|
B2
|
Vysoká aktivita erytrocytární glutathion reduktázy.
u. riboflavin/kreatinin < 11 nmol/mmol
|
Striktní diety, po průjmu, chirurgické operaci, zejm. resekci žaludku, po ATB léčbě,
|
|
Niacin
|
u. N methyl nikotinamid < 2,5 mg/24hod.
|
Převažující kukuřičná strava (bez fermentačního předzpracování).
|
|
B6
|
Vysoká aktivita erytrocytární transaminázy.
|
Těhotenství, užívání estrogenů jako antikoncepce, vysokoproteinová dieta, hypertyreózy, aktinoterapie, omezená resorpce z tenkého střeva.
|
|
Biotin
|
s. biotin < 0,5 nmol/l
|
Konzumenti syrového bílku (avidin).
|
|
K. listová
|
s. k. listová < 3 µg/l
Erytrocytární kyselina listová < 150 µg/l.
|
Těhotenství, laktace, dospělí, užívání antikonvulziv (hydantoináty).
|
|
B12
|
s. B12 < 150 pmol/l
|
Vegetariáni, makrobiotici, po gastrektomii, resekci ilea.
|
|
C
|
Leukocytární C vit. < 0,1 µmol/10 buněk.
|
Kuřáci, hormonální antikoncepce.
|
Vitaminy rozpustné v tucích
Liposolubilní vitaminy (vitamín A, D, E, K) jsou deriváty isoprenů. Jejich účinné vstřebávání je podmíněno nenarušeným vstřebáváním tuk.
Tabulka 17: Vitaminy rozpustné v tucích
|
Průměrná denní potřeba dospělým
|
Funkce
|
Projevy nedostatku
|
Potravinové zdroje
|
|
K
1 µg/1 kg tělesné hmotnosti
|
Kofaktor karboxylačních reakcí
Tvorba hemokoagulačních faktorů (faktor II, VII, IX, X)
Kalcifikace kostí
Oxidativní fosforylace
|
Poruchy krevní srážlivosti
|
Syntetizován mikroflórou střeva.
Zelená listová zelenina, játra.
Méně: mléko, maso, vejce, obiloviny, ovoce a zelenina.
|
|
E
(tokoferoly, α-tokoferol)
8–10 mg α-TE
|
Hlavní lipofilní antioxidační látky, chrání buněčné membrány před oxidačním poškozením – lipoperoxidací, snižují aterogenní agresivitu oxid. LDL částic.
Antiagregační účinky.
Společně s vit. C blokuje endogenní vznik nitrosaminů.
|
Zkrácení doby přežívání erytrocytů (anémie)
Poruchy reprodukce, neurologické poruchy, svalová dystrofie
Snížená antioxidační obrana organismu před volnými radikály (katarakta, Alzheimerova choroba, stárnutí, KVCH.
|
Obilné klíčky, rostlinné oleje, ořechy, tmavě zelená listová zelenina, vnitřnosti, vejce, mléko
Málo vitamínu E má maso, ryby, živočišný tuk, většina ovoce a zeleniny.
|
|
A
(retinol, retinal, retinová kyselina, karotenoidy s vit. A aktivitou)
0,8–1,2 RE
|
Ovlivňuje genetickou informaci.
Nezbytný pro zrak.
Ovlivňuje buněčnou proliferaci a diferenciaci, buněčnou signalizaci, reprodukci a integritu imunitního systému.
Antioxidační vlastnosti při běžných hladinách.
|
Šeroslepost, xeroftalmie, keratomalacie, slepota
Zvýšená vnímavost k infekcím
Poruchy fertility, suchost kůže, nechutenství
|
Retinol (potr. živ. pův.): (játra, žloutek, máslo, mléko)
β karoten: rostlinné pigmenty v červené a žluté zelenině a ovoci a tmavě zelené listové zelenině
|
|
D není typický vitamín, syntetizován v kůži za pomoci UV záření
Ergokalciferol D2
Cholekalciferol D3
0–10 µg
|
Metabolismus kalcia a fosforu: zvyšuje plazmatické hladiny prostřednictvím zvýšení jejich resorpce ve střevě, kosti a zpětného vychytávání ledvinou.
V osifikující části kosti ale stimuluje činnost osteoblastů a mineralizaci kosti.
Má vliv na dělení a diferenciaci buněk včetně imunitního systému.
|
Osteomalacie (dospělost)
Křivice (dětství):
Nervové poruchy, pocení v záhlaví, zuby opožděně prořezávané
Caput quadratum, kraniotabes, pectus carinatum, rachitický růženec, Harrisonova rýha.
|
Rybí tuk, játra, mořské ryby, žloutek, máslo,
Fortifikované výrobky: mléko, margariny
|
α-TE (tokoferolový ekvivalent): 1 mg α-TE = 1 mg přirozeně se vyskytujícího α-tokoferolu. Při převodu ostatních látek s aktivitou vit. E na α-TE je třeba vynásobit jejich množství v mg příslušným faktorem: pro β-tokoferol (*0,5); γ-tokoferol (*0,1), α-tokotrienol (*0,3); syntetický α-tokoferol(* 0,74). Suplementace by neměla překročit 300 IU (200 α-TE ) vit. E denně.
RE (retinolový ekvivalent): 1µg RE = 1 µg všech trans retinolů = 6 µg všech trans β karotenů = 12 µg všech ostatních karotenoidů, které mají aktivitu provitamínu A. Syntetické deriváty vit. A, označované jako retinoidy se většinou uvádějí v mezinárodních jednotkách (IU), kdy 1 IU = 0,3 µg všech trans retinolů.
10 µg vit. D = 400 IU (1 IU = 0,25 µg vit. D)
Tabulka 18: Liposolubilní vitamíny, laboratorní průkaz jejich deficitu
|
Deficit
|
Rizikové skupiny obecně: při poruše absorpce tuků (cystická fibróza, porucha hepatobiliárního systému, malabsorpční stavy…).
|
|
K
|
protrombinový čas (normální koncentrace plazmatického protrombinu: 800–1200 µg/l).
|
Léčení dikumarinovými antikoagulancii,
porucha syntézy vit. K střevní mikroflórou (chronická léčba ATB), staré osoby.
|
|
E
|
s. α-tokoferol < 5,5 mg/l;
dobré antioxidační schopnosti při p. tokoferol/cholesterol > 2,25 µmol/mmol
|
Předčasně narozené děti (riziko retrolentární fibroplázie a intravaskulární hemolýzy).
Pravděpodobně ale není optimální příjem vitamínu E v celé populaci.
|
|
A
|
p. retinol <1,3 µmol/l;
retinol vázající protein < 30 mg/l
|
Zejména dětská populace při hladomorech.
|
|
D
|
p. kalcitriol < 15 pg/ml u dospělých, u dětí <18 pg/ml.
|
Osoby s nedostatečným osluněním a nízkým přívodem D vitamínu v potravě.
|
Toxicita vysokého příjmu vitamínů
Předávkování vit. K vede k bolestem hlavy, horečce, nechutenství, při i. v. aplikaci i k tachykardii a bronchospasmu. U vit. E byla stanovena letální dávka 2 g/1 kg hmotnosti.
V případě vit. A nastává chronická toxicita z příjmu stravou pouze v případě větší konzumace jater nebo oleje z jater ryb. Většinou je ale výsledkem kombinace suplementace a vysokého příjmu. Projevuje se u dospělých při dlouhodobě užívaných denních dávkách 15 mg retinolu (50 000 IU)/den a u dětí 6 mg retinolu (18 000 IU)/den. Spočívá v bolestech hlavy, apatii, nechutenství, zvracení, deskvamaci kůže, kostních změnách a jaterním poškození. Teratogenní účinek s projevy spontánních potratů, malformací lebky, obličeje, srdce, thymu a centrální nervové soustavy byl shledán u plodů, jejichž matky v prvním trimestru gravidity užívaly dávky 0,5-1,5 mg/kg syntetické kyseliny retinové. Z tohoto důvodu by dávka během gravidity neměla přesáhnout 3 mg retinolu (10 000 IU) denně. Akutní toxicita je vyvolána většinou syntetickými preparáty při jednorázové dávce u dospělých 2–5 mil IU/den, transientní toxické projevy pak mohou nastat při 1 mil. IU a chronická toxicita nastává při opakované dávce v množství 300 000 IU /70 kg a den po dobu 7 měsíců.
Nadbytek vit. D vede k vyplavování kalcia z kostí, hyperkalcémii, kalciurii a ukládání vápníku v ledvinách, srdci a cévách. U mladých lidí byla hypervitaminóza D popsána po dávkách 45 µg vitamínu D (1800 IU).
Vysoké dávky vit. C ve formě suplementací mohou mít naopak prooxidační účinky, zvyšují riziko močových oxalátových konkrementů, poškozují vitamín B12 s projevy megaloblastické anemie a u novorozenců, jejichž matky užívaly v graviditě megadávky vitamínu C, vyvolávají skorbut.
Toxické projevy po akutním předávkování kyseliny nikotinové jsou bolesti hlavy, pocity horka a návaly krve do obličeje. Chronické předávkování zhoršuje glukózovou toleranci, jaterní funkce a vede k hyperurikemii.
Nejčastější terapeutické a preventivní využití vitamínů
Niacin v léčbě pelagry a k prevenci hypercholesterolemie. Pyridoxin v léčbě syndromu karpálního tunelu. Vit. B12 k zlepšení kognitivních funkcí. Kyseliny listové k prevenci hyperhomocysteinemie. Vit. C je podáván u skorbutu, dále jako adjuvantní terapie u septického šoku a jako prevence bronchopulmonální dysplázie a intravaskulární hemoragie u předčasně narozených dětí. Donošeným novorozencům se dále jako prevence hemoragické nemoci aplikuje dávka 0,5–1,0 mg vit. K intramuskulárně, nedonošeným minimálně 1 mg. Vit. E se terapeuticky podává v dávce 100-200 mg při léčbě infertility, atrofii sliznic, neurastenii, degeneraci kloubů, onemocnění kůže, myopatiích, cystické fibróze, k prevenci kardiovaskulárních chorob. Vit. D se používá k léčbě osteoporózy a k prevenci křivice.
Minerály – makroelementy
Tabulka 19: Makroelementy (přijímány v denních dávkách nad 100 mg) (s.: sérový; p.: plazmatický; u.: urinární), SD = subklinický deficit.
|
Průměrná denní potřeba dospělým člověkem
|
Biochemická funkce
|
Klinický deficit
|
Markery nutričního stavu s referenčními hodnotami
|
Potravinové zdroje
|
|
Vápník
800–1200 mg
|
Součást kostí a zubů, nervosvalová dráždivost, svalová kontrakce, membránová integrita a transport.
Krevní srážlivost.
|
Osteomalacie, osteoporóza, tachykardie, nervosvalová dráždivost
SD: Kolorektální karcinom? (vazba žlučových kyselin).
|
p. Ca: 2,4–2,7 mmol/l
|
Mléko a mléčné výrobky, obiloviny, luštěniny, listová zelená zelenina- brokolice, kapusta; mák, fortifikované potraviny, měkké kosti ryb – sardinky
|
|
Fosfor
800–1200 mg
|
Součást kostí a zubů
Součást DNA, RNA, ATP, fosfolipidů
|
Těžká svalová slabost, parézy až respirační selhání.
|
p. P: 0,7–1,6 mmol/l
|
Prakticky všechny potraviny, nejvíce ve zdrojích bílkovin, aditivech.
|
|
Hořčík
300–400 mg
|
Intra-, extracelulární kationt.
Kofaktor enzymů (buněčný metabolismus), udržení elektrického potenciálu nervových a svalových membrán, neuromuskulární přenos.
|
Poškození a spasmy cévní stěny, porucha elasticity membrán, tetanie.
Nauzea, svalová slabost, mentální poruchy.
|
p. Mg:
0,65–1,00 mmol/l
|
Nezpracované potraviny: ořechy luštěniny, nemleté obilí, zelenina (součást chlorofylu), brambory
Málo v mase, rybách, mléce, ovoci
|
|
Sodík
500–2400 mg = (1,3–6g soli)
1 mmol Na = 23 mg Na
|
Hlavní extracelulární kationt – udržuje objem extracelulární tekutiny, její osmolaritu, acidobazickou rovnováhu a membránový potenciál buněk.
|
Dehydratace organismu, pokles TK, apatie, křeče
|
p. Na:
132–145 mmol/l
|
Kuchyňská sůl NaCl, při výrobě potravin (75 %), domácí příprava (15 %). 10 % spotřeby formou Na glutamátu a Na bikarbonátu
|
|
Draslík
2500–4000 mg
290 mg = 10 mmol/l
|
Hlavní intracelulární kationt.
Udržování osmotické rovnováhy.
|
Slabost, anorexie, apatie, nauzea. Fatální kardiální arytmie.
|
p. K: 3,8–5,2 mmol/l
|
Zelenina, ovoce, luštěniny, ořechy.
|
|
Chlorid
750 mg a výše
|
Extracelulární aniont.
Udržuje objem extracelulární tekutiny a krve. Udržuje osmotickou rovnováhu. Žaludeční šťáva.
|
Hypochloremická alkalóza.
|
p. Cl: 96–106 mmol/l
|
Kuchyňská sůl, při výrobě potravin. Naturální vody.
|
|
Síra
500–1000 mg
|
Součást AMK: cysteinu, methioninu, glutathionu, detoxikační pochody.
|
|
-
|
Bílkoviny mléka, vajec.
|
Minerály – mikroelementy a stopové prvky
Tabulka 20: Mikroelementy (denní příjem: 1-100mg) a stopové prvky (denní příjem: µg), (s. sérový; p. plazmatický; u. urinární).
|
Průměr. denní potřeba pro dospělého
|
Biochemická funkce
|
Klinický deficit
|
Referenční hodnoty nutričního stavu
|
Potravinové zdroje
|
|
Železo
ženy ve fertilním věku 15–18 mg, muži 10 mg
|
Elektronový transport
Cytochromový systém
Hemoglobin, myoglobin, imunita
|
Anemie mikrocytární. Porucha kognitivních funkcí.
SD: zřejmě nižší rezistence k infekcím
|
s. ferritin: > 12µg/l
s. CRP: < 10 mg/l
|
Játra, maso a masné výrobky s obsahem krve, žloutky, zelenina, ovoce.
|
|
Zinek
10–15 mg
|
Enzymy pro intermediární metabolismus a proteinovou syntézu
Superoxid-dismutáza
Kontrola genové transkripce skrze proteiny
|
Růstová retardace, kožní projevy, ↓ hojení ran, poruchy imunity, únava, ztráta chuti k jídlu
↓ antioxidační obrany
|
p. Zn s albuminem 35–55 g/l a C reaktivním proteinem < 10 mg/l
|
Maso, sýry, vejce, obiloviny, luštěniny.
|
|
Mangan
2–5 mg
|
Koenzym mitochondriální superoxid-dismutázy, arginázy, kofaktor pro hydrolázy, kinázy.
|
Lipidové abnormality
Anemie
|
p. Mn:
7–27nmol/l
|
Ovesné vločky, čaj, kakao, celozrnný chléb.
|
|
Fluor
1,5–4 mg
|
Mineralizace kostí a zubů jako kalcium fluoroapatit
|
Zubní kaz, porucha ukládání vápníku do kostí
|
-
|
Fluoridovaná voda, mořské ryby.
|
|
Měď
2–2,5 mg
|
Koenzym cytochrom-oxidázy, superoxid-dismutázy
Neuroaktivní aminy
|
Hypochromní anemie
Neutropenie
Poruchy imunity, růstu vlasů a nehtů
Subperiostální krvácení
Kard. arytmie
|
p. Cu: 10–25 µmol/l ceruloplasmin: 130–300 mg/l s. CRP: < 10 mg/l
|
Maso, vejce, luštěniny.
|
|
Molybden
150–350 µg
|
Xantinoxidáza v DNA metabolismu. Sulfitoxidáza v S metabolismu.
|
Intolerance S-AMK. Tachykardie, poruchy zraku.
|
-
|
Játra, ledvinky, ovesné vločky, rýže.
|
|
Chrom
50–200 µg
|
Insulinová aktivita, genová exprese, lipoproteinový metabolismus.
|
Glukózová intolerance
Periferní neuropatie
|
p. Cr:
2–10 nmol/l
|
Maso, pivovarské kvasnice, sýry, pšen. klíčky, ořechy
|
|
Jód
150 µg
|
Trijodtyronin, tyroxin –celulární metabolismus
|
Hypothyreoidismus v dospělosti, kretenismus u dětí, struma
|
s. T4: 70–155; s. T3: 1,4–3,2 nmol/l; s. TSH: 0,2–4 mIU/l
|
Mořské ryby a produkty, vejce, mléko, jodidovaná sůl
|
|
Selen
50–100 µg
|
Koenzym glutathion peroxidázy, thyroxin dejodidázy
|
↓antioxidační a imunitní obrany (SD: ↑riziko novotvarů). Myopatie kost. svalu a srdce. Makrocytóza
|
p. Se:
0,8–2,0 µmol/l
|
Mořské produkty, v obilovinách závisí na obsahu Se v půdě
|
|
Kobalt
5–10 µg
|
Součást vitamínu B12
|
Poruchy krvetvorby a neuropatie
|
-
|
Zelenina, celozrnné obiloviny.
|
|
Další stopové prvky: Arsen, Boron, Cín, Křemík, Nikl, Vanad
|
|
Průměr. denní potřeba pro dospělého
|
Biochemická funkce
|
Klinický deficit
|
Referenční hodnoty nutričního stavu
|
Potravinové zdroje
|
Fytochemické látky
Vyskytují se v rostlinné stravě (ovoce, zelenina, luštěniny, obiloviny) a mají biologický účinek na člověka. Patří mezi ně tzv. fytoprotektivní látky (nutriceuticals), které jsou semiesenciální a vykazují antikarcinogenní a antiaterogenní účinky. Přijímány v nadbytku (mimo stravu) však mohou i škodit. Podle své struktury se dělí na:
Tabulka 21: Fytoprotektivní látky
|
Zástupce
|
Účinek:
AA(antiaterogenní)
AK (antikancerogenní)
|
Zdroje
|
|
Flavonoidy a isoflavonoidy--fytoestrogeny
|
Flavonol flavonon flavanol isoflavonoidy katechiny antokyany
|
Antioxidační, a tím AA, dále imunostimulační, antialergické a protizánětlivé úč.; vazbou tranzitních kovů ovlivňují aktivitu enzymů.
AK: Sójové isoflavonoidy (daidzein, genistein) strukturálně podobné estrogenům, snižují pravděpodobně riziko rakoviny prsu a prostaty.
|
Ve všech druzích ovoce (jablka, citrusy, borůvky, aronie) a zeleniny (cibule), čajích, víně, pivu, luštěninách a bramborech
Příjem až 1 g denně
|
|
Chlorofyly
|
Chlorofyl a jeho derivát chlorofylin
|
AK: antimutagenní úč. proti řadě karcinogenů
Tvoří s karcinogeny biolog. inertní komplexy.
|
Zelené rostliny, v listové zelenině 2–600 g/kg sušiny
|
|
Inhibitory proteáz
|
|
AK: mohou potlačit vývoj maligních lézí
Mají biolog. aktivitu trypsinu a chymotrypsinu, brání vzniku reaktivních forem kyslíku z aktivovaných makrofágů (antioxidační úč.)
|
Sója
|
|
Indol a jeho deriváty
|
Glukobrasicin
Indol-3-karbinol
|
AK (indukce isoenzymů cytochromu P450 a stimulace glutathion reduktázy) = biotransformace xenobiotik
|
Křížatá zelenina (kapusta zelí, brokolice, brukev)
|
|
Isothiocyanáty
|
Např. fenetylisothiocyanát
|
Mají jak příznivé, tak nepříznivé úč. na zdraví, inhibují enzymy I. fáze metabolismu xenobiotik (někdy výhoda, která může zabránit vzniku karcinogenu in vivo (např. nitrosaminům) = AK
|
Ostrá a palčivá chuť: křen, ředkvičky, ředkev, řeřicha
|
|
Jednoduché polyfenolové sloučeniny
|
Ellagová, gallová skořicová, kávová kyselina..
|
Antioxidační (AA) i AK (aktivace glutathion transferázy → konjugace a eliminace karcinogenů)
|
Tvoří taniny, třísloviny, jednoduché glykosidy
maliny, jahody, ostružiny
|
|
Karotenoidy
|
600 sloučenin, jen málo z nich má aktivitu vit. A
karoteny α, β.. lykopen, lutein..
|
Antioxidační úč. při norm. příjmu 2–6 mg denně – redukují singletový kyslík (AA, AK –chrání DNA před oxidativní bodovou mutací, pravděpodobně chrání také před kataraktou)
Při dávkách 20 mg/den a vyšších ale riziko prooxidačního úč. a vzniku nádorů u kuřáků
|
Žluté a oranžové části rostlin a plodů, někdy překryty zeleným chlorofylem (natě)
|
|
Sulfidy
|
Diallysulfid, Diallydisulfid ajoen
|
AK: modulace enzymů deaktivující chemické prokarcinogeny), hypocholesterolemický (AA) a antihypertenzní účinek
|
Česnek, cibule
|
|
Terpeny
|
Často součástí prchavých silic
Lemonen
|
AK: inhibice buněčné proliferace, stimulace buněčné diferenciace, indukce enzymů konjugační fáze biotransformací xenobiotik
|
Výrazné aroma, citrusové plody a slupky, aromatické byliny
|
Součástí rostlinné stravy mohou být i fytochemické látky s toxickým účinkem. Kromě hub se jedná o solanin v lilkovitých rostlinách, vyklíčených bramborách, glykosidy odštěpující kyanovodík v mandlích a jádrech peckovin, furokumariny v celeru, pastináku, petrželi, způsobující fotodermatózy.
Protektivní přístup v skladbě a zpracování potravy
Nutno dodat, že podobného protektivního efektu lze dosáhnout i opačným individuálním přístupem ke stravě, kdy nebudeme cíleně vyhledávat ochranné látky, ale naopak zabráníme příjmu potravy s obecně zdravotně škodlivým obsahem. K jeho výskytu do značné míry přispívá i technologická úprava stravy. Rozdíly v prevalenci např. zhoubných nádorů v různých zemích v epidemiologických studiích vchází do souvislosti s určitým výskytem protektivního faktoru, zároveň však i s rozdílným způsobem skladování, konzervování i kuchyňské přípravy. Známým příkladem je vznik nebezpečných transmastných kyselin z jinak zdravých polynenasycených mastných kyselin. Dále uzené a grilované potraviny mohou obsahovat polycyklické aromatické uhlovodíky, z nichž řada z nich jsou prokázané karcinogeny. Při vysokých teplotách mohou vznikat z bílkovin, resp. jejich základních stavebních prvků – aminokyselin – pyrolyzáty (heterocyklické aminy) s mutagenními účinky. Potraviny nasolované, nakládané do dusitanových solících směsí, obsahují dusitany, ze kterých mohou vzniknout v ústech a žaludku za určitých okolností nitrosaminy nebo jiné nitrososloučeniny, podezřívané z karcinogenních účinků. S těmi jsou dávány do souvislosti zejména nádory žaludku a močového měchýře. V důsledku nevhodného skladování potravin může dojít ke kontaminaci a bujení plísní, produkujících karcinogenní produkty – mykotoxiny. Zvýšení expozice aflatoxinům např. zvyšuje riziko vzniku nádorů jater, zejména u osob s chronickými postižení tohoto orgánu. Protektivně pak také působí omezení příjmu tuků na 30 % celkového příjmu energie, konzumace alespoň 400 g čerstvého ovoce a zeleniny a konzumace dostatečného množství vlákniny (část je hrazena ovocem a zeleninou, zbytek potravinami s preferencí celozrnného pečiva, cereálií), omezení konzumace smažených, grilovaných, nasolených, uzených potravin, omezení konzumace alkoholických nápojů (zejména vysokoprocentních).
Výživové doporučené dávky
Výživové doporučené dávky vznikly v USA v roce 1941 a pod názvem “Reccommended dietary allowances“ (RDA) a sloužily jako standardy k předcházení nutričních deficitů. Doporučená dávka je zde definována jako průměrná denní dávka esenciálního nutrientu, o které bylo rozhodnuto konsensem nutricionistů, že je dostatečná k pokrytí známých nutričních potřeb u 97–98 % zdravých lidí z populační skupiny specifikované věkem a pohlavím“. Při konstrukci dávky se vychází z odhadu průměrné fyziologické potřeby nutrientu organismem a jeho navýšením jak o ztráty vzniklé při vstřebávání živiny, tak o tzv. bezpečnostní limit, který tvoří 2 směrodatné odchylky od průměru zohledňující interindividuální rozdíly mezi lidmi. Z důvodu negativního dopadu doporučení vyšší dávky energie než je individuální potřeba se bezpečnostní navýšení v případě doporučení energie neprovádí.
Takto koncipované dávky (viz Obrázek10., vydání z roku 1989) (1) si nenárokují být dávkami individuálně optimálními a z pohledu prevence zejména chronických civilizačních onemocnění jsou nedostatečné. Proto se v současné době pro potřeby plánování a kontrolování stravy zdravých lidí rozpracovává nové vícehodnotové pojetí (2). Nahrazuje pod zastřešujícím označením Výživové referenční příjmy „Dietary reference Intakes“ (DRI) původní koncepci RDA a vymezuje čtyři následovně definované hodnoty:
- Estimated average requirement (EAR) je průměrná dávka příjmu nutrientu, která se na základě experimentálních důkazů jeví jako dostatečná k udržení požadovaných biochemicko - fyziologických funkcí u 50 % zdravých individuí věkově a pohlavím vymezené populace.
- Recommended dietary allowance (RDA) je dávka příjmu esenciálního nutrientu, považovaná na základě vědeckých znalostí jako dostatečná k pokrytí známých nutričních potřeb prakticky všech (97–98 %) zdravých individuí věkově a pohlavím vymezené populace (obvykle EARs +2σ).
- Adequate intake (AI) se užije v případě, že nejsou dostatečné údaje ke stanovení EAR. AI je založen na experimentálně určených aproximacích průměrného přijmu nutrientu definovanou populační skupinou, které se jeví schopné udržet definovaný nutriční stav, ev. růst.
- Tolerable upper limit (UL) je nejvyšší denní dávka příjmu nutrientu, u které je ještě nepravděpodobné, že by zapříčiňovala riziko nežádoucích zdravotních účinků.

Obrázek 2: Dietary Reference Intake
Evropská Unie má od r. 1993 platné „Recommended Dietary Allowances“ (RDA). Byly vypracovány z důvodů jednotných postupů nutričního značení potravin, komunitních výživových programů, vědeckých potřeb a mnoha dalších. Jsou stanoveny pro zdravé osoby rovněž s primárním cílem zabránění projevu deficitu, nikoli tedy zajištění optimální výživy s ohledem na chronické civilizační choroby. Pod zastřešujícím názvem RDA se skrývají rovněž čtyři hodnoty pro nutrient.
- Average requirement (AR): Jde o průměrný denní příjem nutrientu, založený na předpokladu normálního rozložení potřeby nutrientu.
- Population reference intake (PRI)
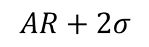
- Lowest threshold intake (LTI)

- Acceptable ranges of intake (ARI): Byl vytýčen pro esenciální nutrienty, u nichž chybí data pro stanovení AR. Byl stanoven pro pantothenovou kyselinu, biotin, vitamin D, sodík, hořčík, mangan.
Pro těhotné, kojící, kojence a děti byla stanovena pouze hodnota PRI, pro staré osoby dávky s výjimkou vitaminu D nebyly specifikovány.
Jako směrná hodnota pro značení potravin v Evropské unii byla stanovena hodnota AR pro dospělé muže, s výjimkou železa, kde byla vybrána AR dospělých žen.
Tabulka 22: Výživová doporučení Evropské unie pro dospělé. U žen, kde dávka není uvedena, je shodná s dávkou pro muže (3).PRI: populační referenční příjem
Eqv = ekvivalent; ARI = Acceptable Range of Intake; TE=tokoferolový ekvivalent; NE=niacinový ekvivalent
|
|
Muži
|
Ženy
|
|
Energy (MJ/d)
|
|
11,3
|
8,5
|
|
Protein (g)
|
PRI
|
0,75 g/kg
|
|
|
Vitamin A (µg)
|
PRI
|
700
|
600
|
|
Vitamin D (µg)
|
ARI
|
0–10
|
|
|
Vitamin E (mg)
|
PRI
|
0,4 mg alfa TE/PUFA
|
|
Riboflavin (mg)
|
PRI
|
1,6
|
1,3
|
|
Niacin (mg niacin ekv.)
|
PRI
|
1,6 mg NE/MJ
|
|
|
Thiamin (mg)
|
PRI
|
100/MJ
|
|
|
Pantothenová kyselina (mg/d)
|
ARI
|
3–12
|
|
|
Vitamin B6
|
PRI
|
15 µg/g proteinu
|
|
|
Vitamin B 12 (µg)
|
PRI
|
1,4
|
|
|
Biotin (µg)
|
ARI
|
15–100
|
|
|
Kyselina listová (µg)
|
PRI
|
200
|
|
|
Vitamin C (mg)
|
PRI
|
45
|
|
|
Vápník (mg)
|
PRI
|
700
|
|
|
Fosfor (mg)
|
PRI
|
550
|
|
|
Hořčík (mg)
|
ARI
|
150–500
|
|
|
Sodík (mg)
|
ARI
|
575–3500
|
|
|
Draslík (mg)
|
PRI
|
3100
|
|
|
Železo (mg)
|
PRI
|
9
|
16
|
|
Zinek (mg)
|
PRI
|
9,5
|
7
|
|
Měď (mg)
|
PRI
|
1,1
|
|
|
Selen (µg)
|
PRI
|
55
|
|
|
Jód (µg)
|
PRI
|
130
|
|
|
Mangan (mg)
|
ARI
|
1–10
|
|
|
n-3 PMK (% energie)
|
PRI
|
0,5
|
|
|
n.6 PMK (% energie)
|
PRI
|
2
|
|
|
|
Muži
|
Ženy
|
SZO má svá doporučení ve formě doporučovaného příjmu (Recommended Intake) a dalších bezpečnostních hodnot, které jsou vysvětleny v legendě k Tabulka 16. Všechna SZO/FAO/UNU doporučení jsou shrnuta v tabulce 17–19 (4,5,6).
Tabulka 23: Výživová doporučení SZO do 6 let věku
|
|
0–3 měsíce
|
3–6 měsíců
|
1–3 roky
|
4–6 let
|
|
Energie MJ/d
|
RI 1975
|
3,4
|
3,4
|
5,7
|
7,6
|
|
Energie kcal
|
RI 1975
|
820
|
820
|
1362
|
1830
|
|
Protein g
|
RI 1975
|
14
|
14
|
16
|
20
|
|
Vitamin A
µg RE/d
|
SLI
|
350
|
350
|
400
|
|
Vitamin D µg
|
RI 1975
|
10
|
10
|
10
|
|
Vitamin B2 mg
|
RI 1975
|
0,5
|
0,5
|
0,8
|
1,1
|
|
Niacin mg
|
RI 1975
|
5,4
|
5,4
|
9
|
12,1
|
|
Vitamin B1 mg
|
|
0,3
|
0,3
|
0,5
|
0,7
|
|
Vitamin B12 µg/d
|
SLI
|
0,1
|
0,1
|
0,5 (1–4 roky)
|
|
Kyselina listová µg/d
|
SLI
|
16
|
24
|
50
|
|
Vitamin C mg
|
RI (1975)
|
20
|
20
|
20
|
|
Vápník g
|
RI (1975)
|
0,5–0,6
|
0,5–0,6
|
0,4–0,5
|
|
Železo mg
|
BR (a)
|
–
|
11 (7–21)
|
6 (4–12)
(1–2 roky)
|
7 (5–14)
(2–6 let)
|
|
Zinek mg
|
LLSR (a)
|
–
|
–
|
5,5 (3,3–11)
(1–3 roky)
|
6,5 (3,9–12,9)
(3–6 let)
|
|
Měď mg/d
|
LLSR
|
0,33–0,55
|
0,37–0,62
|
0,56
(1–3 roky)
|
0,57
(3–6 let)
|
|
Jód µg/d
|
RI
|
50
|
50
|
90
|
Tabulka 24: Výživová doporučení SZO od 7 do 18 let věku
|
7–9 let
Chlapci
|
10–12 let
|
12–15 let
|
15–18 let
|
|
Dívky
|
Chlapci
|
dívky
|
Chlapci
|
dívky
|
|
|
Energie MJ/d
|
RI 1975
|
9,2 (7–9)
|
10,9
|
9,8
|
12,1
|
10,4
|
12,8
|
9,7
|
|
Energie kcal
|
RI 1975
|
2190
|
2600
|
2350
|
2900
|
2490
|
3070
|
2310
|
|
Protein g
|
RI 1975
|
25
|
30
|
29
|
37
|
31
|
38
|
30
|
|
Vitamin A
µg RE/d
|
SLI
|
400
|
500
|
600
|
600
|
500
|
|
Vitamin D µg
|
RI 1975
|
2,5
|
2,5
|
2,5
|
2,5
|
2,5
|
|
Vitamin B2 mg
|
RI 1975
|
1,3
|
1,6
|
1,4
|
1,7
|
1,5
|
1,8
|
1,4
|
|
Niacin mg
|
RI 1975
|
14,4
|
17,2
|
15,5
|
19,1
|
16,4
|
20,3
|
15,2
|
|
Vitamin B1 mg
|
|
0,9
|
1,0
|
0,9
|
1,2
|
1,0
|
1,2
|
0,9
|
|
Vitamin B12 µg/d
|
SLI
|
0,9
|
1
|
1
|
1
|
|
Kyselina listová µg/d
|
SLI
|
102
|
102
|
170
|
|
Vitamin C mg
|
RI (1975)
|
20
|
20
|
30
|
30
|
|
Vápník g
|
RI (1975)
|
0,4–0,5
|
0,6–0,7
|
0,6–0,7
|
0,6–0,7
|
|
Železo mg
|
BR (a)
|
12 (8–23) pro 6–12 let
|
18
(12–36)
|
20
(13–40)
|
18
(12–36)
|
20
(13–40)
|
|
Zinek mg
|
LLSR (a)
|
7,5
(4,5–15)
|
9,3
(5,6–8,7)
|
8,4
(5–16,8)
|
12,1
7,3–24,3
|
10,3
6,1–20,6
|
13,1
7,8–26,2
|
10,2
6,2–20,6
|
|
Měď mg/d
|
LLSR
|
0,75
|
0,73
|
0,77
|
1,0
|
1,33
|
1,15
|
|
Selen µg/d
|
LLSR
|
25
|
30
|
36
|
30
|
40
|
30
|
|
Jód µg/d
|
RI
|
120
|
120
|
150
|
150
|
Tabulka 25: Výživová doporučení SZO pro těhotenství a laktaci
hodnoty železa pro ženy ve fertilním věku 24 (16–48) mg , v klimakteriu 9 (6–19) mg
RI = recommended intake doporučovaný příjem
RE = retinolový ekvivalent
SLI = (safe level of intake) bezpečná hladina příjmu
LLSR = lower limits of safe ranges of population intakes for normative values normativní hodnoty spodních limitů bezpečného pásma populačního příjmu
BR = (basal requirement) základní potřeba (oblasti vysoké a nízké biologické dosažitelnosti)
ASR = acceptable safe range (1mg/d =ENR) přijatelná bezpečná oblast
|
|
Muži
|
Ženy
|
Těhotenství
|
Laktace
|
|
Energie MJ/d
|
RI 1975
|
12,6
|
9,2
|
+1,5
|
+2,3
|
|
Energie kcal
|
RI 1975
|
3000
|
2200
|
+350
|
+550
|
|
Protein g
|
RI 1975
|
37
|
29
|
38
|
46
|
|
Vitamin A
µg RE/d
|
SLI
|
600
|
500
|
600
|
850
|
|
Vitamin D µg
|
RI 1975
|
2,5
|
2,5
|
10
|
10
|
|
Vitamin B2 mg
|
RI 1975
|
1,8
|
1,3
|
+0,2
|
+0,4
|
|
Niacin mg
|
RI 1975
|
19,8
|
14,5
|
+0,2
|
+3,7
|
|
Vitamin B1 mg
|
|
1,2
|
0,9
|
+0,1
|
+0,2
|
|
Vitamin B12 µg/d
|
SLI
|
1
|
1
|
1,4
|
1,3
|
|
Kyselina listová µg/d
|
SLI
|
200
|
170
|
370–470
|
270
|
|
Vitamin C mg
|
RI (1975)
|
30
|
30
|
50
|
50
|
|
Vápník g
|
RI (1975)
|
0,4–0,5
|
0,4–0,5
|
1,0–1,2
|
1,0–1,2
|
|
Železo mg
|
BR (a)
|
11
8–23
|
–
|
–
|
13
9–26
|
|
Zinek mg
|
LLSR (a)
|
9,4
5,6–18,7
|
6,5
4–13,1
|
7,3–9,3–13,3*
4–26,7
|
12,7–11,7–9,6**
7–25,3
|
|
Měď mg/d
|
LLSR
|
1,35
|
1,15
|
1,15
|
1,25
|
|
Selen µg
|
LLSR
|
40
|
30
|
39
|
46
|
|
Jód µg/d
|
RI
|
150
|
150
|
200
|
200
|
|
Molybden µgkg TH/d
|
BR
|
0,4
|
0,4
|
|
|
|
Chrom µg/d
|
ENR
|
33
|
33
|
|
|
|
Nikl µg/d
|
BR
|
<100
|
<100
|
|
|
|
Boron mg/d
|
ASR
|
1–13
|
1–13
|
|
|
|
Vanad mg/d
|
BR
|
10
|
10
|
|
|
* hodnoty pro 1.–2. a 3. trimestr
** hodnoty pro první 3, další 4.–9. měsíc a posledních 10–12 měsíců laktace
Tabulka 26: Nutriční referenční hodnoty uvedené v Codex Alimentarius (7):
|
Nutrient
|
Jednotky
|
NRV
|
|
Protein
|
µg
|
50
|
|
Vitamin A
|
µg
|
800
|
|
Vitamin D
|
µg
|
5
|
|
Vitamin C
|
mg
|
60
|
|
Vitamin B1
|
mg
|
1,4
|
|
Vitamin B2
|
mg
|
1,6
|
|
Niacin
|
mg
|
18
|
|
Vitamin B6
|
mg
|
2
|
|
Kyselina listová
|
µg
|
1
|
|
Vápník
|
mg
|
800
|
|
Hořčík
|
mg
|
300
|
|
Železo
|
mg
|
14
|
|
Zinek
|
mg
|
15
|
|
Jód
|
µg
|
150
|
České Výživové doporučené dávky (VDD)
Poslední verze vypracovaná Státním zdravotním ústavem byla vydaná v roce 1993 (8) (tabulka 21–23). Jde u energie a vybraných živin (bílkoviny, sacharidy, tuky, vápník, železo, kyselina linolová, vitaminy A, B1, B2, C, E) vždy pouze o jednu doporučovanou hodnotu pro věkem, pohlavím a fyzickou aktivitou vymezenou populační skupinu. Zvlášť jsou vyčísleny VDD pro těhotné a kojící ženy. VDD jsou vždy po několika letech revidovány, kdy se na základě nově získaných poznatků, event. podle odlišné interpretace dosavadních výsledků, upřesňují VDD nově. V současné době jsou rozpracovány návrhy na nové hodnoty VDD, které musí projít schvalovacím řízením.
Tabulka 27–29: Příklad českých výživových doporučených dávek Převzato podle (8).
Tabulka 27
|
Výživový faktor
0–6
|
Kojenci
Měsíce
|
|
Děti předškolního věku – roky
Chlapci
Dívky
|
Děti školního věku – roky
|
Dospívající 15–18 let
|
|
7–10
1–3
|
Chlapci
|
Dívky
|
|
|
|
|
7–12
|
4–6
|
|
11–14
|
11–14
|
Studující
|
Fyzicky
pracující
|
Studující
|
Fyzicky
pracující
|
|
|
Energie
|
KJ
|
2600
|
3600
|
5500
|
7000
|
9000
|
10500
|
9500
|
11500
|
12500
|
9000
|
10000
|
|
Kcal
|
620
|
860
|
1315
|
1670
|
2150
|
2510
|
2270
|
2745
|
2985
|
2150
|
2390
|
|
Bílkoviny
|
g
|
20
|
30
|
45
|
60
|
75
|
90
|
80
|
95
|
105
|
75
|
85
|
|
Tuky
|
g
|
30
|
30
|
40
|
55
|
65
|
75
|
70
|
85
|
95
|
65
|
75
|
|
Sacharidy
|
g
|
68
|
117
|
193
|
234
|
316
|
368
|
330
|
400
|
428
|
316
|
343
|
|
Kyselina linolová
|
g
|
3
|
3,5
|
4,5
|
5,5
|
7,5
|
9
|
8,5
|
10
|
11
|
9
|
10
|
|
Vápník
|
mg
|
700
|
900
|
900
|
900
|
1100
|
1200
|
1200
|
1200
|
1200
|
1200
|
1200
|
|
Železo
|
mg
|
8
|
10
|
10
|
12
|
14
|
16
|
18
|
18
|
18
|
18
|
20
|
|
Vit. A
|
ug
|
400
|
400
|
400
|
500
|
700
|
900
|
900
|
1000
|
1000
|
900
|
900
|
|
Vit. B1
|
mg
|
0,2
|
0,5
|
0,5
|
0,7
|
1
|
1,2
|
1,1
|
1,3
|
1,5
|
1
|
1,1
|
|
Vit. B2
|
mg
|
0,4
|
0,7
|
0,8
|
1
|
1,3
|
1,7
|
1,6
|
2
|
2,2
|
1,5
|
1,6
|
|
Vit. C
|
mg
|
50
|
50
|
50
|
55
|
60
|
80
|
80
|
100
|
110
|
90
|
100
|
|
Vit. E
|
mg
|
5
|
6
|
6
|
8
|
10
|
12
|
10
|
14
|
15
|
12
|
12
|
|
B
T
S
|
12,9
|
14
|
13,7
|
14,4
|
14
|
14,4
|
14,1
|
13,8
|
14,1
|
14
|
14,2
|
|
43,4
|
31,5
|
27,4
|
29,6
|
27,2
|
26,9
|
27,8
|
27,9
|
28,6
|
27,2
|
29,3
|
|
43,7
|
54,5
|
58.9
|
56
|
58,8
|
58,7
|
58,1
|
58,3
|
57,3
|
58,8
|
57,5
|
Tabulka 28
|
Výživový faktor
|
|
Ženy
|
|
Pracující 19–34 let
|
Těhotné od II. trimestru
|
Kojící
|
Pracující 35-54 let
|
Nepracující
|
|
|
Práce
|
Práce
|
55-74 let
|
75 a více let
|
|
|
Lehká
|
Střední
|
Těžká
|
Lehká
|
Střední
|
Těžká
|
|
|
Energie
|
KJ
|
9000
|
10000
|
11000
|
11000
|
12000
|
8500
|
9000
|
10000
|
8000
|
7000
|
|
Kcal
|
2150
|
2385
|
2625
|
2625
|
2865
|
2030
|
2150
|
2385
|
1910
|
1670
|
|
Bílkoviny
|
g
|
70
|
75
|
80
|
90
|
100
|
65
|
70
|
75
|
65
|
60
|
|
Tuky
|
g
|
65
|
75
|
85
|
75
|
90
|
60
|
65
|
75
|
55
|
50
|
|
Sacharidy
|
g
|
321
|
352
|
385
|
398
|
413
|
308
|
310
|
353
|
289
|
245
|
|
Kyselina linolová
|
g
|
7
|
8
|
9
|
9
|
9
|
7
|
8
|
9
|
7
|
7
|
|
Vápník
|
mg
|
800
|
800
|
800
|
1500
|
2000
|
800
|
800
|
800
|
700
|
700
|
|
Železo
|
mg
|
16
|
16
|
18
|
28
|
24
|
16
|
16
|
18
|
12
|
10
|
|
Vit. A
|
ug
|
900
|
900
|
900
|
1100
|
1200
|
900
|
900
|
900
|
800
|
750
|
|
Vit. B1
|
mg
|
1
|
1.1
|
1.2
|
1.2
|
1.4
|
1.1
|
1.2
|
1.4
|
1.1
|
1
|
|
Vit. B2
|
mg
|
1.4
|
1.6
|
1.7
|
1.6
|
1.8
|
1.4
|
1.5
|
1.6
|
1.4
|
1.2
|
|
Vit. C
|
mg
|
75
|
75
|
90
|
120
|
130
|
75
|
75
|
90
|
75
|
75
|
|
Vit. E
|
mg
|
12
|
14
|
16
|
14
|
18
|
12
|
14
|
16
|
12
|
12
|
|
B
T
S
|
13
|
12.6
|
12.2
|
13.7
|
14.0
|
12.8
|
13.0
|
12.6
|
13.6
|
14.4
|
|
27.2
|
28.3
|
29.1
|
25.7
|
28.3
|
26.6
|
27.3
|
28.3
|
25.9
|
27
|
|
59.8
|
59.1
|
58.7
|
60.6
|
57.7
|
60.6
|
59.7
|
59.1
|
60.5
|
58.6
|
Tabulka 29
|
Výživový faktor
|
|
Muži
|
|
Pracující 19-34 let
|
Pracující 35-59 let
|
Nepracující
|
|
|
Práce
|
55-74 let
|
75 a více let
|
|
|
Lehká
|
Střední
|
Těžká
|
Lehká
|
Střední
|
Těžká
|
|
|
Energie
|
KJ
|
11000
|
12000
|
14000
|
10000
|
11500
|
13000
|
9000
|
8000
|
|
Kcal
|
2625
|
2685
|
3345
|
2385
|
2745
|
3105
|
2150
|
1910
|
|
Bílkoviny
|
g
|
80
|
85
|
100
|
75
|
80
|
95
|
70
|
65
|
|
Tuky
|
g
|
75
|
85
|
105
|
70
|
80
|
100
|
60
|
55
|
|
Sacharidy
|
g
|
408
|
440
|
499
|
364
|
426
|
457
|
333
|
289
|
|
Kyselina linolová
|
g
|
8
|
9
|
10
|
8
|
8
|
10
|
8
|
8
|
|
Vápník
|
mg
|
800
|
800
|
800
|
800
|
800
|
800
|
700
|
700
|
|
Železo
|
mg
|
14
|
16
|
18
|
14
|
16
|
18
|
12
|
10
|
|
Vit. A
|
ug
|
1000
|
1000
|
1000
|
1000
|
1000
|
1000
|
850
|
800
|
|
Vit. B1
|
mg
|
1.1
|
1.2
|
1.4
|
1
|
1.2
|
1.4
|
1.2
|
1
|
|
Vit. B2
|
mg
|
1.6
|
1.8
|
2.1
|
1.5
|
1.7
|
2
|
1.4
|
1.3
|
|
Vit. C
|
mg
|
75
|
90
|
100
|
75
|
90
|
100
|
75
|
75
|
|
Vit. E
|
mg
|
12
|
14
|
16
|
12
|
14
|
16
|
12
|
12
|
|
B
T
S
|
12.2
|
11.9
|
12
|
12.6
|
11.7
|
12.2
|
13
|
13.6
|
|
25.7
|
26.7
|
28.3
|
26.4
|
26.2
|
28.9
|
25.1
|
25.9
|
|
62.1
|
61.4
|
59.7
|
61
|
62.1
|
58.9
|
61.9
|
60.5
|
Využití VDD je mnohostranné. Slouží jako standardy pro označování a uvádění nutričních hodnot potravin, pro suplementaci a fortifikaci potravin potravními doplňky a při vývoji a výrobě nových potravin a doplňků stravy. Vychází se z nich při plánování výživové politiky a zásobování obyvatelstva potravinami, při celodenním stravování v sociálních zařízení, včetně armády, vězeňství; jako podklady jsou nezbytné ve školním stravování (včetně mateřských škol a jeslí), v závodních jídelnách, při sestavování terapeutických diet v nemocnicích. Slouží jako srovnávací kritéria při epidemiologických studiích, monitoringu nutričního příjmu populačních skupin pro identifikaci vysoce rizikových skupin obyvatelstva, ev. pro vyhledávání rizikových nutrientů. Zohledňují se při tvorbě ozdravných výživových programů, nutriční edukaci atd.
Metody vyšetřování nutričního stavu
Při vypracovávání vhodných preventivních i léčebných intervenčních programů v oblasti životního stylu (zejména optimální výživou a pohybovou aktivitou) je klíčovým výchozím bodem vstupní individuální analýza stravovacích a pohybových zvyklostí a vyšetření a znalost všech komponent tzv. zdravotně orientované tělesné zdatnosti – tj. i nutričního (výživového) stavu. Nutriční stav se však vyšetřuje nejen pro účely individuální intervence, ale i při populačních studiích, kdy získaná data umožňují sledovat vývoj výživového stavu specifických populačních skupin či celé populace a přijímat vhodná opatření na úrovni ochrany a podpory veřejného zdraví.
Anamnestické možnosti sledování vývoje nutričního stavu a analýzy příjmu živin
Ve všech lékařských oborech je důkladná anamnéza nenahraditelným zdrojem informací o pacientovi/klientovi a o jeho životním stylu, o sociálním i materiálním prostředí, kterým je obklopen.
Nutriční stav zcela zásadně souvisí se zdravotním stavem jedince, výstižné je označení „zdravotně nutriční stav“. Optimální nutriční stav je dán energeticky i nutričně vyváženým příjmem potravy, fyziologickým vstřebáváním a využíváním všech jejích složek, včetně nenutričních, ale zdraví prospěšných komponent výživy, zároveň s dodržením podlimitního a zdraví nepoškozujícího příjmu aditiv a kontaminantů. Při komplexní anamnéze zaměřené na vývoj nutričního stavu se snažíme odhalit osobní (tj. osobnostní, zdravotní, sociální i pracovní) a rodinná rizika vývoje možných malnutričních stavů. A to nejen ve smyslu vývoje nadváhy či obezity, ale vždy i se zřetelem na rizika karence makronutrientů i mikronutrientů při nevhodném životním stylu či při závažném onemocnění. U jedinců závislých na péči jiné osoby, nebo při podezření na neúplnost a nepřesnost uváděných údajů se vždy pokoušíme ověřit relevantnost získaných informací u rodinných příslušníků nebo jiných pečujících osob.
Zaměření zejména:
- v rodinné anamnéze na genetickou zátěž obezitou či podváhou, kardiovaskulárním onemocněním, arteriální hypertenzí, diabetes mellitus 2. typu, nádorovými onemocněními
- v osobní anamnéze:
- na porodní hmotnost a stav výživy v dětství, během dospívání, vývoj hmotnosti v dospělosti (rychlost a záměrnost nebo nezáměrnost velkých váhových změn, jejich okolnosti)
- u žen na gynekologickou anamnézu (menarche, fyziologie cyklu, váhové změny v souvislosti s užíváním hormonální antikoncepce, těhotenstvím, kojením a menopauzou)
- u mužů na andrologickou anamnézu (hypogonadální stav)
- na předchozí i stávající onemocnění (omezení fyzické aktivity či změna stravovacích zvyklostí ze zdravotních důvodů; závažné úrazy a prodělané operace; závažná onemocnění a jejich terapie; časté infekce; již dříve diagnostikované malnutrice, komorbidity obezity, jejich terapie)
- na subjektivní vnímání současného stavu (celkové příznaky – např. zvýšená unavitelnost, psychické potíže, obtížné kousání, polykání, gastrointestinální příznaky – nechutenství, nauzea, nezbytnost a četnost užívání antacid, projímadel)
- na sociální a pracovní anamnézu (závažné životní situace a jejich prožívání; kuřácké návyky, pokusy zanechat kouření; pracovní zátěž fyzická i psychická, směnný provoz s vlivem na stravovací zvyklosti; poruchy spánku)
- v nutriční anamnéze:
- na stávající stravovací zvyklosti (chuťové preference, pestrost stravy, vyhýbání se některým potravinovým komoditám, četnost a velikost porcí během dne, pravidelnost, rychlost konzumace jídla, vynechávání některých denních zvyklých jídel, jezení v noci, „zajídání“ stresu, přejídání se; konzumace alkoholu; dostupnost potravin sociální a/nebo ekonomická – hladovění, sociální izolace, stravování doma, veřejné stravování, restaurace, rychlé občerstvení,…)
- na potravinové alergie, intolerance
- na užívání doplňků stravy, specifické diety, alternativní způsoby výživy (vegetariánství, makrobiotika, vliv tradic, náboženství – „zakázané potraviny“,…)
- na poruchy příjmu potravy (varovné příznaky mentální anorexie, bulimie – deprese, výčitky po konzumaci jídla, přísné hlídání energetického příjmu, záchvaty přejídání se, podrážděnost, uzavření se do sebe,…)
- odhad energetického a nutričního složení přijímané potravy (např. využití softwaru NutriDan, pro vědecké účely pro přesné stanovení vybraných nutrientů pak použití např. metody chemické analýzy dvojité porce)
Energetické a nutriční vyhodnocování jídelníčků softwarem NutriDan
Nutriční software NutriDan je program vyvinutý za podpory Institutu Danone v roce 2003 MUDr. Danou Müllerovou, Ph.D. z Ústavu hygieny a preventivní medicíny Lékařské fakulty UK v Plzni, a jejími spolupracovníky Ing. Zbyňkem Tychtlem, Ph.D. (ZČU Plzeň), doc. Ing. Luďkem Müllerem, Ph.D. (ZČU Plzeň) a prof. MUDr. Zuzanou Brázdovou, DrSc. (MU Brno). V současné době je k dispozici aktualizovaná verze softwaru NutriDan II (2010).
NutriDan je široce využíván na různých odborných pracovištích po celé ČR. Představuje uživatelský program určený do rukou odborníka – nutričního terapeuta, diabetologa, obezitologa, lékaře v poradně výživy. Není určen pro laickou veřejnost, protože výsledky potřebují další popis, zhodnocení a vysvětlení. Program obsahuje databázi stovek potravin, jejichž složení vychází z literárních údajů českých receptur školního stravování, a jejichž nutriční hodnota byla prověřena na Ústavu hygieny a preventivní medicíny Lékařské fakulty Univerzity Karlovy v Plzni. Hodnoty jsou uváděny pro jedlý podíl, nezahrnují však ztráty během skladování, při tepelné úpravě, konzervaci apod.
Tento software umožňuje dlouhodobé sledování vývoje stravovacích návyků pacientů a vyhodnocení jídelníčků. Vypočítává průměrný denní příjem živin s ohledem na pohlaví, věk, nutriční stav a míru fyzické aktivity jednotlivce (BMI, těhotenství, kojení) s možností vytvoření energeticky vyváženého jídelníčku. Při použití tohoto programu má odborník možnost analýzy jednodenního nebo vícedenního jídelníčku. Jídelníček je sumární, což znamená, že v případě zadávání více dnů není možné provést analýzu jednotlivých dnů. Toto je třeba si rozhodnout před započetím zadávání jídelníčku.
Do databáze mohou autoři přidávat nové potraviny, u kterých lze údaje opravovat nebo mazat. Jako zdroj dat lze využít On-line databázi složení potravin ČR, která je k dispozici na internetové adrese http://www.czfcdb.cz.
Složení zadávaných potravin či jídel je možné zobrazit.
Program v jídelníčku analyzuje energetický příjem a zastoupení základních makronutrientů (sacharidů, lipidů a proteinů) a mikronutrientů (vitamínů, minerálů, stopových prvků) a porovnává je s individuálně vypočítávanými referenčními hodnotami. Automaticky nastaví hodnoty makronutrientů, kdy obsah proteinů je 0,8 g na 1 kg hmotnosti (u obezity na 1 kg optimální hmotnosti). Tuky by měly představovat maximálně 30 % celkového energetického příjmu (u pacientů nad 3 roky). Zbylou dávku energie tvoří sacharidy. Také hodnoty mikronutrientů se nastavují automaticky na základě populačního referenčního příjmu podle Evropské unie.
Výsledky z vyšetření se znázorňují sloupcovými grafy nebo ve formě výpisu protokolu, kde jsou porovnávány výsledné hodnoty s doporučenými, popřípadě ve formě potravinové pyramidy. Ve formě protokolu a pyramidy jsou data prezentována pacientům.
a) Při zadávání potravin vzniká sloupcový graf, kde se jednotlivé nutrienty obsažené v jídle sčítají. Konkrétní potraviny a jídla jsou barevně identifikovatelné (viz Obr. 4).

Obrázek 3: Zobrazení sloupcového grafu živin v softwaru NutriDan
b) Program NutriDan shrne výsledky do protokolu, kde je u jednotlivých nutrientů ve sloupcích uveden jejich skutečný příjem klientem, doporučená dávka, a z ní vypočtený procentuální příjem, kterého klient dosáhl (viz Obr. 5, 6).
Obrázek 4
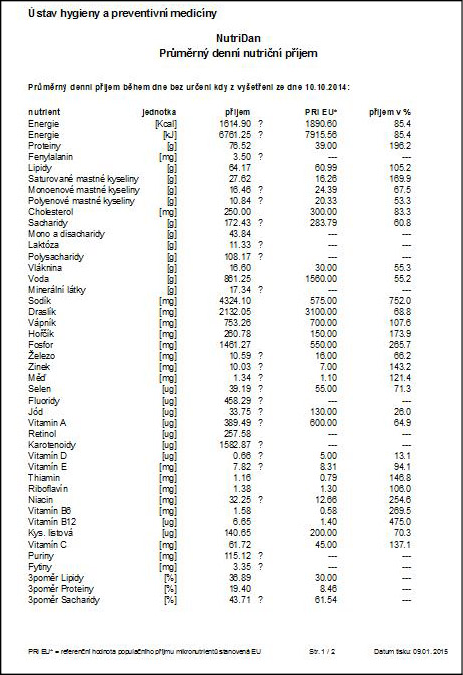
Obrázek 5: Zobrazení protokolu přijatých živin v softwaru NutriDan
c) Pro názornější vysvětlení analýzy jídelníčku pacientovi je k dispozici potravinová pyramida, přičemž pyramida vlevo je pyramida s doporučeným příjmem potravy a pyramida vpravo znázorňuje skutečné pacientovo stravování (viz Obr. 6).
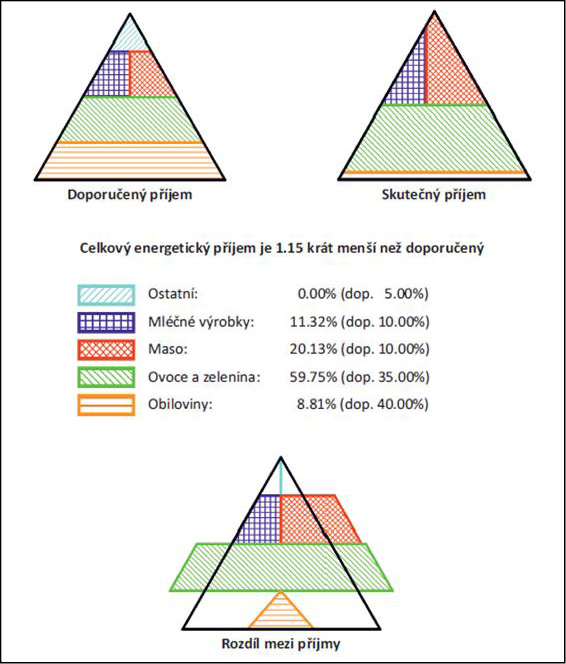
Obrázek 6: Zobrazení pyramidy přijatých živin v softwaru NutriDan
Interpretace výsledků při použití programu NutriDan II
Hodnoty nutrientů včetně dávky bílkovin odpovídají referenčním dávkám Evropské unie PRI EU specifikovaným pro věk a pohlaví. Tyto hodnoty pro jednotlivé nutrienty označuje u sloupcových grafů zelená linie. Spodní červená linie představuje 75 % a horní červená linie 125 % populační referenční hodnoty připadající vyšetřovanému na 1 den.
V případě energie je referenční hodnota odvislá od výživového stavu vyšetřovaného (podvýživa, nadváha, obezita), od fyzické aktivity, stáří a pohlaví.
U nadváhy a obezity zjištěné podle BMI u dospělého je korekce pro energetickou dávku vypočítána z energetické dávky odvozené od horního limitu ideální hmotnosti při dané výšce a věku, korigované faktorem pro fyzickou aktivitu a snížením této dávky o 1/3. Při podvýživě naopak navýšením o 1/3 energetické dávky odpovídající aktuálnímu věku, pohlaví, hmotnosti, fyzické aktivitě. Nadváha nebo obezita je posuzována podle BMI, nikoli podle měřeného zastoupení tělesného tuku. To znamená, že nutriční poradce koriguje výpočet v případě kulturistů (BMI vyšší než 25, ale nejedná se o obezitu) a v případě starších lidí, kdy jejich mírná nadváha podle BMI také nutně neznamená aplikaci energeticky redukční diety navrhované počítačem.
Navrhovaná dávka energie pro obézní děti a děti s podvýživou (nad 90. či pod 10. percentilem rozložení BMI) v programu NutriDan vychází z výpočtu potřebné energie, vypočítané z bazálního energetického výdeje připadajícího na dítě daného věku, pohlaví a dále údaje tělesné výšky a hmotnosti odpovídající 50. percentilu rozložení BMI v české populaci a je korigována faktorem fyzické aktivity.
Zvláštní hodnoty mají pak těhotné či kojící ženy.
Bílkoviny by měly být v pásmu zelené linie a výše, a neměly by přesahovat dvojnásobek hodnoty určené zelenou linií (t. j. PRI pro bílkoviny).
Tuky by naopak neměly převyšovat zelenou linii, neměly by však klesnout pod 25 % celkového energetického příjmu (viz graf Energetický trojpoměr živin v NutriDanu). Při hodnocení spektra tuku (viz graf Tuky, cholesterol) mohou přesahovat zelenou linii pouze monoenové tuky (mastné kyseliny s jednou dvojnou vazbou), ostatní by měly být pod linií.
Vitamíny, minerály a vláknina by měly převýšit alespoň zelenou linii. To neplatí u vitamínu A a D, kdy vitamín A nemá stejnou variabilitu v každodenním příjmu a vitamín D je tvořen v kůži po expozici slunečnímu záření. U vitamínu C se musí počítat spíše s nadhodnocením přijaté dávky, neboť se nezohledňují jeho ztráty skladováním potravin apod.
Příjem selenu a jódu není vzhledem k použité metodice relevantní (nepřesný odhad soli, obsah selenu a jódu je závislý na jejich obsahu v půdě, na které byly potraviny vyprodukovány).
V programu NutriDan je stanovená dosti přísně hodnota pro obsah sodíku v potravě. Literatura uvádí denní příjem soli pod 5 g, tedy pod 2 g sodíku, ale program NutriDan doporučuje mnohem menší množství a to 575 mg. Toto množství se nemění pro dospělé ženy ani muže a neovlivňuje ho věk či fyzická aktivita.
Klientovi po vyhodnocení stravovacího záznamu je pak možné doporučit náležitou úpravu stravovacích zvyklostí např. s využitím rámcových kaloricky definovaných jídelníčků, viz následující ukázky:
Jídelníček 6300 kJ (1500 kcal)
Celkově za den sníst:
Tabulka 30: Vzorový jídelníček pro 6300 kJ (1500kcal)
|
Zelenina: 4 porce po 100–150 g
|
|
Obiloviny: 3 porce
Ekvivalent jedné porce:
30–50 g nevařených celozrnných obilovin (ovesné kaše apod.)
1 ks celozrnného pečiva (40–50 g)
ovocný koláč 40–50 g (v případě např. perníku 25 g)
Příloha: ½ běžné porce (80 g vařených (těstovin, rýže, knedlíků), 120 g brambor, bramborové kaše)
|
|
Luštěniny nebo ořechy a semena: 1 porce
Ekvivalent jedné porce:
100 g vařených luštěnin
15–20 g ořechů nebo semen
|
|
Ovoce: 2–3 porce
Ekvivalent 1 porce:
100 g syrového ovoce
50 g konzervovaného ovoce s cukrem
20 g sušeného ovoce
|
|
Maso, ryby, drůbež: 1–2 porce (je-li pouze 1 porce, pak 2. musí být nahrazena luštěninami nebo mléčným výrobkem)
Ekvivalent 1 porce:
80 g libového masa
120 g rybího masa
2 vejce
|
|
Mléko a mléčný výrobek: 1–2 porce (je-li pouze 1 porce, pak 2. musí být nahrazena 1 porcí ze skupiny Maso, ryby, drůbež (nebo mléčným výrobkem)
Ekvivalent 1 porce:
250 ml nízkotučný mléčný výrobek
150 ml neodtučněný mléčný výrobek
30–50 g sýr (30 g tučný, 50 g 30% a méně tuku v sušině)
|
|
Tuky: 3 porce po 10 g z toho alespoň 2 porce z olejů
|
|
Mlsy: max. 1 porce za den
čokoláda 10 g
alkohol: 1 dcl, vína nebo 250 ml piva nebo malá odlivka tvrdého alkoholu
sušené ovoce 20 g
müsli tyčinka 15 g
další porce tuku 10 g nebo cukru 10 g
|
Jídelníček 7560 kJ (1800 kcal)
Celkově za den sníst:
Tabulka 31: Vzorový jídelníček pro 7560 kJ (1800 kcal)
|
Zelenina: 4 porce po 100–150 g
|
|
Obiloviny: 5 porcí
Ekvivalent jedné porce:
30–50 g nevařených celozrnných obilovin (ovesné kaše apod.)
1 ks celozrnného pečiva (40–50 g)
ovocný koláč 40–50 g (v případě např. perníku 25 g)
Příloha: ½ běžné porce (80 g vařených těstovin, rýže, knedlíků, 120 g brambor, bramborové kaše)
|
|
Luštěniny nebo ořechy a semena: 1 porce
Ekvivalent jedné porce:
100 g vařených luštěnin
15–20 g ořechů nebo semen
|
|
Ovoce: 2–3 porce
Ekvivalent jedné porce:
100 g syrového ovoce,
50 g konzervovaného ovoce s cukrem
20 g sušeného ovoce
|
|
Maso, ryby, drůbež: 1–2 porce (je-li pouze 1 porce, pak 2. musí být nahrazena luštěninami nebo mléčným výrobkem)
Ekvivalent jedné porce:
80 g libového masa
120 g rybího masa
2 vejce
|
|
Mléko a mléčný výrobek: 2 porce (je-li pouze 1 porce, pak 2. musí být nahrazena1 porcí ze skupiny Maso, ryby, drůbež (nebo mléčným výrobkem)
Ekvivalent jedné porce:
250 ml nízkotučný mléčný výrobek,
150 ml neodtučněný mléčný výrobek
30–50 g sýr (30 g tučný, 50 g 30% a méně tuku v sušině)
|
|
Tuky: 3 porce po 10 g z toho alespoň 2 porce z olejů
|
|
Mlsy: max. 1 porce za den
čokoláda 10 g
alkohol: 1 dcl, vína nebo 250 ml piva nebo malá odlivka tvrdého alkoholu
sušené ovoce 20 g
müsli tyčinka 15 g
další porce tuku 10 g nebo cukru 10 g
|
Jídelníček 9240 kJ (2200 kcal)
Celkově za den sníst:
Tabulka 32: Vzorový jídelníček pro 9240 kJ (2200 kcal)
|
Zelenina: 4 porce po 100–150 g
|
|
Obiloviny: 7 porcí
Ekvivalent jedné porce:
30–50 g nevařených celozrnných obilovin (ovesné kaše apod.)
1 ks celozrnného pečiva (40–50 g)
ovocný koláč 40–50 g (v případě např. perníku 25 g)
Příloha: ½ běžné porce (80 g vařených těstovin, rýže, knedlíků, 120 g brambor, bramborové kaše)
|
|
Luštěniny nebo ořechy a semena: 2 porce
Ekvivalent jedné porce:
100 g vařených luštěnin
15–20 g ořechů nebo semen
|
|
Ovoce: 2–3 porce
Ekvivalent jedné porce:
100 g syrového ovoce
50 g konzervovaného ovoce s cukrem
20 g sušeného ovoce
|
|
Maso, ryby, drůbež: 1–2 porce (je-li pouze 1 porce, pak 2. musí být nahrazena luštěninami (nebo mléčným výrobkem)
Ekvivalent jedné porce:
80 g libového masa
120 g rybího masa
2 vejce
|
|
Mléko a mléčný výrobek: 2 porce (je-li pouze 1 porce, pak 2. musí být nahrazena 1 porcí ze skupiny Maso, ryby, drůbež mléčným výrobkem)
Ekvivalent jedné porce:
250 ml nízkotučný mléčný výrobek
150 ml neodtučněný mléčný výrobek
30–50 g sýr (30 g tučný, 50 g 30% a méně tuku v sušině)
|
|
Tuky: 4 porce po 10 g z toho alespoň 2 porce z olejů
|
|
Mlsy: max. 2 porce za den
čokoláda 10 g
alkohol: 1 dcl, vína nebo 250 ml piva nebo malá odlivka tvrdého alkoholu
sušené ovoce 20 g
müsli tyčinka 15 g
další porce tuku 10 g nebo cukru 10 g
|
Ukázky postupu chemické analýzy vybraných nutrientů
Zkrácené orientační stanovení některých nutričních hodnot pokrmů.
Zpracování vzorku pokrmu
- Celá porce se zváží; je-li příliš suchá (pod 20 % vlhkosti), přidá se voda v poměru 1 : 0,5.
- Pokrm se zhomogenizuje mixováním v kuchyňském mixéru.
- Do dvou 100 ml baněk (nebo kádinek) A a B se odváží po 5 g homogenátu.
- Zapíše se přesná hmotnost homogenátu.
Příprava extraktů z potravin pro následné analýzy
Baňka A – stanovení celkového obsahu tuků a cholesterolu
Baňka B – stanovení obsahu chloridů, kyseliny askorbové, celkový obsah fenolů a polyfenolů, celková antioxidační kapacita metodou FRAP, obsah jednoduchých cukrů
Chemikálie a pracovní roztoky:
Folchovo extrakční činidlo (chloroform + methylalkohol v poměru 2 : 1)
Extrakční směs methylalkohol + voda v poměru 1 : 1
Postup:
- Pro extrakt z baňky A používáme pouze skleněné zkumavky, pro extrakt z baňky B můžeme používat zkumavky plastové.
- Homogenát v baňce A doplníme do 25 g Folchovým extrakčním činidlem (potravina má být s extrakční směsí v poměru přibližně 1 : 4).
- Homogenát v baňce B se přelije 12 ml extrakční směsi methylalkohol- voda 1 : 1.
- Uzavřeme zátkou a důkladně protřepeme (min. 3 min). Můžeme mírně zahřívat pro lepší extrakci.
- Směs můžeme buď přendat do zkumavek a odstředit (4 000 otáček po dobu 1 min) anebo přefiltrovat.
Laboratorní analýzy
Extrakt A – stanovení celkového obsahu tuků a cholesterolu
Stanovení celkového obsahu tuků
Postup:
- 2 ml odstředěného extraktu se pipetuje na předem zváženou odpařovací misku (na 2 desetinná čísla)
- Odpaří se do sucha při teplotě 100–105 stupňů C.
- Po ochlazení se zváží.
Výpočet:
Od hmotnosti misky s odparkem se odečte hmotnost prázdné odpařovací misky. Získáme hmotnost odparku = hmotnost tuku ve 2 ml extraktu.
Protože 25 ml extraktu obsahovalo 5 g vzorku → 2 ml extraktu obsahuje 0,4 g vzorku.
0,4 g vzorku obsahují hmotnost tuku, která se rovná hmotnosti odparku, např. 0,047 g.
Např. 0,4 g vzorku …………. 0,047 g tuku
100 g vzorku ………… x g tuku
x = 11,75 g (= Vzorek pokrmu obsahuje 11,75 % tuku)
Stanovení obsahu cholesterolu
Chemikálie a pracovní roztoky:
- Standardní roztok cholesterolu 0,5 % (25 mg cholesterolu + 50 ml chloroformu)
- Chloroform
- Acetanhydrid
- Kyselina sírová konc.
Postup:
- 1 ml extraktu se v 10 ml zkumavce odpaří (opatrně lze v digestoři ve vodní lázni nad kahanem)
- Do stojánku na zkumavky si připravíme další 2 zkumavky (pro standard a pro slepý vzorek)
- V první zkumavce máme odpařený extrakt (vzorek), ve druhé zkumavce 0,1 ml standardního roztoku cholesterolu a ve třetí zkumavce 0,1 ml chloroformu.
- Do každé zkumavky se přidají 2 ml chloroformu, 0,5 ml acetanhydridu a 0,1 ml konc. kyseliny sírové.
- Promícháme na vortexu
- Ponecháme stát 10 minut v temnu
- Spektrofotometricky při 625 nm se vyhodnocuje intenzita vzniklého zeleného zbarvení proti slepému vzorku (destilovaná voda). Použijeme skleněné kyvety.
Extrakt B – stanovení obsahu chloridů, kyseliny askorbové, celkový obsah fenolů a polyfenolů, celková antioxidační kapacita metodou FRAP, obsah jednoduchých cukrů
Obsah chloridů podle Mohra – argentometrie (je ekvivalentní obsahu sodíku)
Chemikálie a pracovní roztoky:
5% roztok chromanu (nebo dichromanu) sodného
Carezzovo činidlo I a II – komerční výrobky
0,1 M standardní roztok dusičnanu stříbrného
0,1 M standardní roztok NaCl
Princip:
AgNO3 + NaCl → AgCl↓ + NaNO3
2 AgNO3 + K2CrO4 → Ag2CrO4↓ + 2 KNO3
Vzniká červená sraženina Ag2CrO4, která je však rozpustnější než AgCl, a proto se začne vylučovat až po úplném vysrážení halogenidů.
pH roztoku musí být 6,5–10,5.
Postup:
- Do baňky pipetovat 6 ml extraktu vzorku.
- Přidat destilovanou vodu (takové množství, aby nám šlo baňkou dobře míchat)
- Přidat 2 ml roztoku chromanu sodného
- Titrovat roztokem dusičnanu stříbrného do vzniku čokoládově hnědého zbarvení.
- (Je-li extrakt příliš zakalený, vyčeří se před titrací přidáním 0,3 ml Carezza I a 0,3 ml Carezza II, přefiltruje se nebo odstředí.)
- Spotřebě 1 ml titračního roztoku odpovídá 0,1 mmolu Na (tj. 2,3 mg).
Obsah kyseliny askorbové (vitamínu C) – Tillmansova titrace
Chemikálie a pracovní roztoky:
- 2% roztok kyseliny octové
- 0,001 M vodný roztok 2,6-dichlorfenolindofenolu
- Standardní roztok kyseliny askorbové – 10 µg KA / 1 ml
Princip:
Kyselina askorbová je oxidována roztokem 2,6-dichlorfenolindofenolu, který tím přechází na bezbarvou leukobázi. Jeho nadbytek vytváří v kyselém prostředí červené zbarvení.
Postup:
- Do baňky pipetovat 5 ml extraktu.
- Přidat 1 ml roztoku kyseliny octové.
- Titrovat roztokem 2,6-dichlorfenolindofenolu do vzniku prvního růžového zabarvení.
- Paralelně 5 ml standardního roztoku kyseliny askorbové – tím se získá tzv. faktor DFIF, který se použije k výpočtu při dalších titracích.
Celkový obsah fenolů a polyfenolů
Chemikálie a pracovní roztoky:
- Folinovo činidlo – komerční výrobek
- nasycený vodný roztok uhličitanu sodného – 7,5 g + 95 ml vody
- standardní roztok kyseliny gallové – 10 mg + 100 ml vody
Postup:
- Připravíme si 3 zkumavky.
- Do každé zkumavky se pipetuje 1 ml vody + 1 ml Folinova činidla (zředěného vodou 1:3).
- Do první zkumavky přidáme 50 µl extraktu vzorku, do druhé kyselinu gallovou (standard), do třetí destilovanou vodu (slepý vzorek).
- Promíchá se na vortexu.
- Po 5 minutách se přidá 1 ml roztoku uhličitanu sodného.
- Promíchá se.
- Během 10 minut vzniká modré zbarvení, jehož intenzita je úměrná obsahu fenolových látek.
- Hodnotíme spektrofotometricky.
Celková antioxidační kapacita – stanovení metodou FRAP
Chemikálie a pracovní roztoky:
- 0,2 M fosfátový pufr pH 6,5
- standardní roztok kyseliny gallové – 10 mg + 100 ml vody
- 1% vodný roztok ferrikyanidu draselného
- 5% vodný roztok kyseliny trichloroctové
- 0,1% vodný roztok chloridu železitého
Postup:
- Připravíme si 3 zkumavky.
- Do každé napipetujeme 0,95 ml fosfátového pufru.
- Do první zkumavky napipetujeme 50 µl vzorku, do druhé kyselinu gallovou (standard), do třetí destilovanou vodu (slepý vzorek).
- Dále přidáme do každé zkumavky 0,5 ml roztoku ferrikyanidu draselného.
- Promícháme na vortexu.
- Zahříváme 10 minut na 50 stupňů C.
- Do každé zkumavky přidáme 0,2 ml roztoku chloridu železitého a 0,25 ml roztoku kyseliny trichloroctové.
- Promícháme.
- Po 15 min. vzniká modré zbarvení, jehož intenzita je úměrná antioxidační kapacitě vzorku (přepočítává se na µg nebo mg kyseliny gallové).
- Hodnotíme spektrofotometricky – při 700 nm.
Celkový obsah jednoduchých cukrů
Lze stanovit v extraktu vzorku refraktometricky.
Klinické vyšetření nutričního stavu
Základní klinické fyzikální vyšetření výrazně přispívá ke správnému vyhodnocení nutriční stavu. Vyšetření pohledem (aspekcí) a pohmatem (palpací) doplňujeme antropometrickým vyšetřením (změření výšky, hmotnosti a vybraných obvodových charakteristik) a výpočtem hmotnostního indexu. Pro zjištění zdravotních rizik spojených s malnutricí je nezbytné doplnit tato vyšetření o měření krevního tlaku, stanovení obsahu a rozložení tukové tkáně v těle a doplňující laboratorní vyšetření a další specializovaná vyšetření jako např. stanovení klidového energetického výdeje.
V případě podvýživy se v našich podmínkách nejčastěji jedná o kombinaci projevů proteino-energetické malnutrice a nedostatku základních minerálů a vitamínů jako např. železa, zinku, vitamínů A, B2, B6, C a D při nedostatečném příjmu nebo zvýšené potřebě při septických stavech, zánětech nebo nádorových onemocněních. Převážně proteinová malnutrice (kwashiorkor) bývá častější u dětí, kdy při nedostatečném příjmu bílkovin je ještě dostačující pokrytí energetických nároků převážně sacharidovými zdroji.
I u obézních jedinců se zároveň můžeme setkat se známkami podvýživy, jako je např. svalová atrofie, chronické záněty apod.
Aspektivní a palpační vyšetření příznaků malnutrice
- možné příznaky podvýživy:
- u proteino-energetické podvýživy: zpomalené psychomotorické tempo, patrná kachexie (vyhublost) – vymizelý podkožní tuk, atrofie svalstva (málo svalové hmoty a ochablost svalů), chladné, cyanotické končetiny, dušnost při anémii, záněty koutků úst a sliznic dutiny ústní, větší kazivost zubů, suché, lomivé vlasy i nehty, vypadávání vlasů, bledost a suchost kůže, pigmentace, deskvamace, snadný vznik modřin, petechie, folikulární hyperkeratóza, snížený turgor kůže, šeroslepost, zánět nebo suchost spojivky, záněty okrajů očních víček, zvětšení štítné žlázy při nedostatku jódu, deformovaný skelet při rachitis (křivici) zapříčiněné nedostatkem vitamínu D v období růstu kostí
- u převážně proteinové malnutrice: relativně zachovalá svalová hmota a vzhledem k věku může být i normální hmotnost, ale hypoalbuminemické otoky a zvětšená játra, celkové neprospívání dítěte – až mentální a psychomotorická retardace
- možné příznaky u nadváhy a obezity: dušnost, patrné zmnožení vrstvy podkožního tuku, někdy zároveň atrofie svalstva – svalová slabost, odlišná distribuce tuku – převážně gynoidní nebo androidní (někdy obtížné odlišení tuku na břiše od ascitu), často vadné držení těla, omezená pohyblivost, vadné postavení v kloubech dolních končetin, lipodystrofické změny, překrývání kožních laloků, intertrigo a mykózy, strie, projevy hormonální dysbalance – gynekomastie u mužů, hypogonadismus, hypertrichóza u žen, známky chronické žilní insuficience, lymfedém
Antropometrické metody a hmotnostní index BMI, metody stanovení tělesného složení a distribuce tukové tkáně
Antropometrické metody mají výhodu neinvazivnosti, časové a ekonomické nenáročnosti, možnosti využití v terénu, slouží jako podklad pro stanovení morfologické charakteristiky těla, složení těla a distribuce tuku v těle. Jsou však zatíženy subjektivní chybou vyšetřujícího, proto je nezbytné vždy postupovat dle standardizovaných metod a vyšetřující osoba musí být náležitě edukována. Základní dva sledované antropometrické znaky jsou:
- tělesná výška (tj. vzdálenost nejvyššího bodu na hlavě od podložky, měřeno v maximálně vzpřímeném spatném stoji u svislé stěny, hlava se nesmí zaklánět ani předklánět, paty se dotýkají stěny, proband je bez bot, přesnost: 0,5 cm) resp. délka těla (měřeno vleže u dětí do 18–24 měsíců, temeno hlavy se dotýká svislé plochy u nulového bodu měřidla, dolní končetiny jsou natažené, paty se dotýkají druhého svislého konce měřidla, lze použít tzv. korýtko neboli „bodymetr“)
- tělesná hmotnost (tj. hmotnost probanda jen ve spodním prádle, bez obuvi, k měření požíváme kalibrované osobní váhy, položené na pevném podkladu, přesnost: 0,5 kg; děti do 18 měsíců vážíme na kojenecké váze, jen s plenou, jejíž hmotnost se odečítá, přesnost: 0,1 kg)
Pomocí těchto základních antropometrických ukazatelů lze vyhodnotit hmotnostní indexy. Dnes nejčastěji používaný je body mass index (BMI = hmotnost v kg / výška v m2), jako v praxi běžně použitelný ukazatel podváhy, normální hmotnosti, nadváhy či obezity. Koreluje s nemocností a úmrtností nejvíce z používaných indexů. Kritéria pro dospělé jsou stanovena Světovou zdravotnickou organizací.
Tabulka 33: BMI klasifikace hmotnosti pro dospělé
|
Klasifikace podle BMI
|
pásmo BMI (kg/m2)
|
|
Podváha
|
< 18,4
|
|
Normální váha
|
18,5–24,9
|
|
Nadváha
|
25–29,9
|
|
Obezita
|
I. stupeň
|
30–34,9
|
|
II. stupeň
|
35–39,9
|
|
III. stupeň
|
40 a více
|
BMI i tzv. hmotnostně-výškový poměr lze využít i pro hodnocení nutričního stavu dětí, po vztažení individuálních hodnot k referenčním údajům.
Další využívané antropometrické ukazatele a metody sloužící k určení proporcionality těla a distribuce tuku
Obvodové charakteristiky:
- obvod pasu (nejběžněji používaná obvodová charakteristika sloužící ke stanovení distribuce tuku a zároveň k určení míry zdravotního rizika daného centrální distribucí tuku – měří se pásovou mírou, ve střední vzdálenosti mezi dolním okrajem žeber a hřebenem kosti kyčelní, dříve byl používán poměr obvodů: pas/boky nebo pas/ stehno)
- obvod boků (měří se v místě největšího vyklenutí hýždí)
- obvod stehna (měří se horizontálně na nejvyšším místě stehna)
- obvod nedominantní paže (měří se v poloviční vzdálenosti mezi akromionem a olecranonem, po odečtení tloušťky kožní řasy nad tricepsem lze využít pro hodnocení svalové hmoty)
Tabulka 34: Obvod pasu a kardiovaskulární riziko
|
Pohlaví
|
Obvod pasu (cm)
|
Zdravotní riziko
|
|
Muži
|
94–102
|
zvýšené
|
|
> 102
|
vysoké
|
|
Ženy
|
80–88
|
zvýšené
|
|
> 88
|
vysoké
|
Příklady metod sloužící ke stanovování množství tuku v těle, jeho distribuci a jednotlivých tělesných komponent
- Měření tloušťky kožní řasy:
- Jedná se o antropometrickou metodu, která umožňuje stanovit výpočtem z naměřeného množství podkožního tuku celkový obsah tuku v těle. Pomocí kontaktního měřidla kaliperu měříme tloušťku kožní řasy na předem definovaných místech (dle vybrané metodiky se používá různý počet kožních řas: např. 4 kožní řasy: 1. nad tricepsem, 2. nad bicepsem, 3. pod dolním úhlem lopatky, 4. na břiše).
- Měření tělesného složení bioelektrickou impedancí (BIA):
- Nejčastěji v současnosti používaná, neinvazivní a finančně dostupná metoda pro vyhodnocení jednotlivých tkání v organismu z hlediska obsahu vody. Po změření odporu těla, který se mění dle obsahu vody a tuku (tuková tkáň je téměř nevodivá, aktivní tělesná tukuprostá hmota má vysoký podíl vody a elektrolytů, je dobrým vodičem), se vypočte obsah tuku v těle. V České republice jsou dostupné přístroje několika specializovaných výrobců, dvousvodové nebo čtyřsvodové. Vždy je třeba důsledně dodržovat předepsaný způsob měření, tak aby nedocházelo ke zkreslení výsledků. Jejich použití je vhodné ke sledování nutričního stavu i stavu hydratace. Pro děti je však nutno využívat speciální software.
- Hydrodenzitometrie:
- Referenční, dnes však již méně používaná metoda ke stanovení tuku. Je nutná výrazná spolupráce vyšetřovaných jedinců: vážíme jedince na vzduchu, pak ve vodě a změříme reziduální objem plic, denzitu těla a obsah tuku v těle pak vypočteme dosazením změřených hodnot do příslušné rovnice.
- DEXA:
- Jedná se o radiodiagnostickou metodu, založenou na principu odlišné absorpce rtg záření o dvou různých energiích, různými tkáněmi. Lze stanovit obsah tuku, netukové tkáně a kostní denzity. A pomocí speciálních softwarových programů i distribuci tukové tkáně v oblasti břicha a boků.
- CT (computerová tomografie), NMR (nukleární magnetická rezonance):
- Zátěžové metody, používané spíše výjimečně za účelem podrobného vyšetřování a stanovování podílu podkožního a itraabdominálního tuku.
Laboratorní vyšetření biochemických ukazatelů
- k odhalení komorbidit nadváhy a obezity,(z venózní krve: glykémie, jaterní testy, lipidogram, urea, kreatinin, CRP; z moči – mikroalbuminurie při poškození ledvin při DM
- k odhalení nutričních karencí vzniklých např. po opakovaných nutričně nevyvážených restrikčních dietách (např. mikrocytární anémie při nedostatku železa, snížená celková bílkovina, snížení počtu lymfocytů u snížené imunitní odpovědi atd.)
- screening thyreopatie (TSH)
- doplňující vyšetření při podezření na sekundární obezitu (např. hladiny hormonů jako jsou androgeny u hyperandrogenního syndromu u žen, estrogeny u hyperestrogenismus u mužů, hladina inzulinu při inzulinomu, hladina prolaktinu u hyperprolaktémie, volný kortizol v moči u Cushingova syndromu, atd.)
- opakované kontroly během redukčního programu – dle stavu pacienta (při velkých váhových redukcích např. dynamika koncentrace sérových bílkovin, krevní obraz, metabolismus železa, vit. B12, kyselina listová, dusíkové metabolity v séru a moči, mineralogram)
Specializovaná vyšetření obézních pacientů
- EKG a vyšetření kardiorespirační kapacity před zahájením redukčního programu s pravidelnou pohybovou aktivitou viz
- psychologické vyšetření s následným psychologickým poradenstvím
- vyšetření nepřímou kalorimetrií pro zjištění klidového energetického výdeje: stanovení respiračního kvocientu (RQ = VCO2/ VO2) změřením spotřeby kyslíku a výdeje oxidu uhličitého v l/min; čím vyšší kvocient, tím vyšší utilizace sacharidů (RQ ≥ 1) při RQ kolem 0,7 převaha oxidace tuků – lipolýza a hladovění
Specifika hodnocení nutričního stavu u dětí
Pro posouzení, zda somatický vývoj dítěte odpovídá jeho věku a pro vyhodnocení jeho nutričního stavu pomocí BMI, porovnáváme aktuálně změřené tělesné charakteristiky dítěte s doporučenými referenčními hodnotami pro danou populaci, pro příslušný věk a pohlaví. Měření jednotlivců pak musí probíhat v souladu s metodami, které byly použity při získávání referenčních údajů, aby nedošlo ke zkreslení interpretace výsledků.
Referenční (standardní) údaje reprezentují vzorek dané dětské populace, jsou „populační normou“. Tyto údaje jsou získávány způsobem transverzálním, longitudinálním nebo semilongitudinálním. Při transverzálním výzkumu jsou v jednom časovém okamžiku zaznamenány údaje velkých reprezentativních souborů (desetitisíce náhodně vybraných jedinců v konkrétních souborech). Longitudinální způsob umožňuje sledovat vybraný soubor jedinců po delší časové období. Jedná se o menší soubory – několik desítek jedinců pro každé pohlaví. Výhodou je zachycení individuálních změn během růstu, nevýhodou větší časová a organizační náročnost. Semilongitudinální studie jsou kombinací výše uvedených dvou druhů výzkumu – během kratšího časového úseku je sledováno větší množství jedinců.
Celosvětově 25 zemí, včetně České republiky, využívá ke sledování růstu a nutričního stavu dětí národní standardy, tj. data získaná na základě sledování dostatečně reprezentativního vzorku dětské populace na národní úrovni. Referenční údaje poskytuje i WHO. Data pro referenční údaje WHO jsou získávána z mezinárodních multicentrických studií.
Data získaná uvedenými způsoby jsou pak statisticky zpracována (je zjištěna standardní odchylka, tj. rozptyl hodnot kolem průměru) a použita pro tvorbu matematicky upravených percentilových grafů tělesných charakteristik. Viz http://www.szu.cz/publikace/data/seznam-rustovych-grafu-ke-stazeni
Percentilové grafy pro sledování tělesné výšky, hmotnosti, obvodových rozměrů nebo BMI mají na vodorovné ose zaznamenány věkovou škálu, na svislé ose pak hodnoty výšky v cm nebo hmotnosti v kg, popř. hodnoty kg/m2. Graf hmotnostně-výškového poměru je konstruován bez ohledu na věk. Všechny grafy jsou sestavovány zvlášť dle pohlaví. Aby byly grafy přehlednější, bývají členěny na dvě části dle věku (od 0 do 24 nebo 36 měsíců a od dvou nebo tří let do osmnácti let), vzhledem k častějším preventivním prohlídkám a častějšímu měření v novorozeneckém, kojeneckém a batolecím období.
V grafech jsou znázorněny hodnoty hlavních percentilů (3., 10., 25., 50., 75., 90., 97.). Hodnota daného percentilu (pro určitý věk) znamená, že dané procento referenční populace dosáhne této hodnoty a hodnot nižších. Čím větší vzdálenost od 50. percentilu, tím jsou hodnoty sledovaného znaku extrémnější.
Do příslušného percentilového grafu v průběhu růstu dítěte zakreslujeme individuální aktuálně naměřené hodnoty sledovaných antropometrických znaků (spojením jednotlivých hodnot získáváme individuální křivku). Dle pozice dítěte v příslušném percentilovém pásmu pak můžeme hodnotit aktuální stav a vývoj vybrané antropometrické charakteristiky či nutričního stavu pomocí BMI.
Bez porovnání individuální aktuálně dosažené hodnoty BMI se správnými referenčními údaji, bychom dle BMI nemohli nutriční stav dětí hodnotit, protože kritéria pro nutriční stav dítěte (vyjádřeno v absolutních hodnotách BMI) jsou odlišné od kritérií daných WHO pro dospělou populaci. Pokud tedy např. hodnota BMI 5letého chlapce bude 18 (tj. podváha u dospělých) bude u něj stanovena nadměrná hmotnost (nadváha), protože jeho pozice v percentilovém grafu je nad 90. percentilem.
Tabulka 35: Percentilové normativy u dětí
|
Percentilové pásmo
|
Postava dle výšky
|
Jedinec dle hmotnostně-výškového poměru nebo BMI
|
|
nad 97. percentilem
|
velmi vysoká
|
obézní
|
|
nad 90. percentilem
|
s nadměrnou hmotností (nadváhou)
|
|
mezi 75. a 90. percentilem
|
vysoká
|
robustní
|
|
mezi 25. a 75. percentilem
|
střední
|
proporcionální
|
|
mezi 3. a 25. percentilem
|
malá
|
štíhlý (pod ١٠. percentilem: podváha)
|
|
pod 3. percentilem
|
velmi malá
|
hubený
|
Pro průběžnou aktualizaci referenčních údajů byly v České republice prováděny od r. 1951 celostátní (transversální) antropologické výzkumy dětí a mládeže každých deset let. Zatím poslední data byla získána při VI. celostátním antropologickém výzkumu (CAV) dětí a mládeže z roku 2001 (SZÚ, UK PřF, P.Bláha, J.Vignerová, 2004). Pro aktualizované grafy byla tato data použita jako referenční. Protože se však za posledních 10 let zvýšil podíl dětí s nadváhou a obézních jedinců, použitím aktuálních hodnot BMI by se zmírnily normy pro určení odchylky od normální hmotnosti (došlo by k posunu 90. a 97. percentilu k vyšším hodnotám proti r. 1991). Proto byly ponechány v platnosti percentilové grafy BMI z r. 1991.
Velmi pozorně je potřeba posuzovat vývoj hmotnosti kojených dětí. Aktuálně využívané grafy v ČR byly sestrojeny na podkladě společného měření dětí kojených i nekojených. České referenční grafy tělesné délky i obvodu hlavy odpovídají růstu kojených dětí, ale vývoj hmotnosti je jiný. V prvních měsících po porodu mají kojené děti větší hmotnostní přírůstky (individuální křivka stoupá strměji) než děti nekojené. Mezi 2. a 3. měsícem se tento trend zpomaluje, kojené děti se stávají štíhlejšími. Toto však není důvod k zavedení dokrmu, naopak je potřeba dále matku podporovat ve výlučném kojení do 6 měsíců věku dítěte, které je preventivním faktorem rozvoje obezity.
Pomocí percentilových grafů lze posuzovat i to, zda dítě v průběhu svého růstu dosahuje geneticky determinovaného potenciálu. Tzv. predikovaná výška podle výšky rodičů je vymezena následujícím pásmem (vymezující hodnoty se zakreslí na pravou svislou osu percentilového grafu a vytvoří se pásmo souběžné s příslušnou percentilovou čárou): střed mezi skutečnou výškou rodiče téhož pohlaví a výškou rodiče opačného pohlaví zvětšenou /matka-syn/ nebo zmenšenou /otec-dcera/ o 13 cm) +/- 8,5 cm. Jestliže individuální růstová křivka dítěte probíhá v mezních percentilových pásmech, pak určení geneticky predikovaného vzorce růstu může pomoci odlišit poruchu růstu (růstovou retardaci zapříčiněnou nevyhovující výživou, nemocí či zanedbáváním dítěte nebo nadměrný růst) od jeho fyziologické varianty dané vrozenými předpoklady.
Pro kompletní a objektivní posouzení výživového stavu dítěte a včasného odhalení rizika podvýživy nebo naopak rozvoje obezity, posouzení její tíže, příčin a komplikací (mimo jiná doplňující vyšetření upřesňující např. podíl tukové tkáně v těle a její distribuci) současně sledujeme vždy rodinnou anamnézu, socioekonomickou situaci a schopnost rodiny uspokojovat základní potřeby dítěte, stravovací zvyklosti a pohybovou aktivitu dítěte. Nefyziologicky rychlé přírůstky, popř. úbytky hmotnosti mohou mít i organickou příčinu. Hypothyreóza, Cushingův syndrom, deficit růstového hormonu mohou být příčinou obezity. Nepřiměřené hubnutí se může objevit při některých tumorech CNS, malabsorbčních syndromech a některých metabolických onemocněních jako je např. diabetes mellitus.
Ke zkreslení správného posouzení stavu výživy dítěte dle BMI může dojít v případě, že vyšetřovaný jedinec je konstitučně robustní s extrémní muskulaturou. V těchto případech je pak třeba přesně stanovit podíl tukové tkáně k netukovým tělesným komponentám.
Pohybová aktivita v prevenci chronických neinfekčních chorob hromadného výskytu
Význam optimální pohybové aktivity pro primární prevenci civilizačních onemocnění a poruch podpůrně pohybového systému
Člověk je morfologicky i funkčně adaptován na způsob života, ve kterém byla základním předpokladem úspěšného přežití dobrá tělesná zdatnost. Denně při získávání potravy a obraně své sociální skupiny podával fyzické výkony střední až vysoké intenzity. Fylogeneticky jsme přizpůsobeni bipedální vzpřímené lokomoci, střídavému, rovnoměrnému zatížení statickou a dynamickou zátěží. Avšak současný životní styl nejméně většiny světové populace je charakterizován obrovským poklesem fyzické aktivity. Objevuje se pohybový deficit a pohybová chudost „sedící populace“. V pracovním procesu, při transportu i ve volném čase je typické nadměrné, dlouhodobé udržování statických poloh (většinou v nefyziologickém zakřivení páteře a asymetrickém zatížení kloubů horních i dolních končetin) a nedostatek dynamické zátěže střední intenzity. Celosvětově k fyzické nečinnosti přispívá vysoká hustota obyvatel, zvýšená úroveň kriminality, vysoká hustota provozu, nízká kvalita ovzduší, nedostatek parků, cyklostezek a sportovních rekreačních zařízení. Za rizikové populační skupiny nejvíce ohrožené nedostatkem pohybu jsou považovány: ženy a senioři, děti a mladiství a osoby se speciálními potřebami. Každá populační skupina má jiné požadavky na intenzitu, délku a typ pohybové aktivity, tak aby byla splněna kritéria pro optimální pohybovou aktivitu, která má pozitivní vliv na zdraví jedince. Nicméně pohyb má nezastupitelný význam v ontogenezi každého člověka. Formativně ovlivňuje vývoj a funkci všech orgánů a systémů organismu.
Očekávaným efektem optimalizace pohybové aktivity netrénované populace je zvýšení úrovně zdravotně orientované zdatnosti, nikoliv snaha o dosažení maximální fyzické výkonnosti bez ohledu na možné zdravotní komplikace.
Optimální pohyb by měl pozitivně ovlivňovat nejen kardiorespirační a neurohumorální systém, ale podporovat i optimální tvar a funkci podpůrně pohybového sytému: tj. udržovat svalovou rovnováhu a fyziologické postavení obratlů páteře, přispívat k současné optimální pružnosti a pevnosti všech kloubních spojení. Pohybová aktivita z pohledu primární prevence by neměla přetěžovat žádné složky podpůrně pohybového aparátu ani organismus jako celek. Cílem je přispět pohybovou aktivitou k úspěšné funkční i morfologické adaptaci na zátěž prostředím.
Nedostačující (a během života jedince většinou postupně se snižující) úroveň tělesné zdatnosti, vyplývající z nedostatečné pohybové aktivity se rozhodující měrou podílí na vzniku nejen metabolických, kardiovaskulárních a nádorových onemocnění, ale i na vzniku a rozvoji poruch podpůrně pohybového aparátu.
Pokud chceme docílit, aby námi doporučovaná pohybová aktivita byla „ individuálně optimální“, je nezbytné při její preskripci vycházet jak z aktuálního zdravotního stavu jedince, tak i z individuální analýzy stávající pohybové aktivity a funkčních i morfologických komponent zdravotně orientované tělesné zdatnosti.
Mezi funkční komponenty fyzické zdatnosti řadíme:
- kardiorespirační zdatnost (schopnost přijímat, transportovat a využívat kyslík)
- neuromuskulární zdatnost (svalová síla, flexibilita, kvalita základních posturálních a pohybových stereotypů)
Pro objektivní posouzení strukturálních (morfologických) komponent využíváme antropometrické a další metody, které slouží k vyhodnocování výživového stavu jedince.
Význam optimální pohybové aktivity pro primární prevenci civilizačních onemocnění a poruch podpůrně pohybového systému
Člověk je morfologicky i funkčně adaptován na způsob života, ve kterém byla základním předpokladem úspěšného přežití dobrá tělesná zdatnost. Denně při získávání potravy a obraně své sociální skupiny podával fyzické výkony střední až vysoké intenzity. Fylogeneticky jsme přizpůsobeni bipedální vzpřímené lokomoci, střídavému, rovnoměrnému zatížení statickou a dynamickou zátěží. Avšak současný životní styl nejméně většiny světové populace je charakterizován obrovským poklesem fyzické aktivity. Objevuje se pohybový deficit a pohybová chudost „sedící populace“. V pracovním procesu, při transportu i ve volném čase je typické nadměrné, dlouhodobé udržování statických poloh (většinou v nefyziologickém zakřivení páteře a asymetrickém zatížení kloubů horních i dolních končetin) a nedostatek dynamické zátěže střední intenzity. Celosvětově k fyzické nečinnosti přispívá vysoká hustota obyvatel, zvýšená úroveň kriminality, vysoká hustota provozu, nízká kvalita ovzduší, nedostatek parků, cyklostezek a sportovních rekreačních zařízení. Za rizikové populační skupiny nejvíce ohrožené nedostatkem pohybu jsou považovány: ženy a senioři, děti a mladiství a osoby se speciálními potřebami. Každá populační skupina má jiné požadavky na intenzitu, délku a typ pohybové aktivity, tak aby byla splněna kritéria pro optimální pohybovou aktivitu, která má pozitivní vliv na zdraví jedince. Nicméně pohyb má nezastupitelný význam v ontogenezi každého člověka. Formativně ovlivňuje vývoj a funkci všech orgánů a systémů organismu.
Očekávaným efektem optimalizace pohybové aktivity netrénované populace je zvýšení úrovně zdravotně orientované zdatnosti, nikoliv snaha o dosažení maximální fyzické výkonnosti bez ohledu na možné zdravotní komplikace.
Optimální pohyb by měl pozitivně ovlivňovat nejen kardiorespirační a neurohumorální systém, ale podporovat i optimální tvar a funkci podpůrně pohybového sytému: tj. udržovat svalovou rovnováhu a fyziologické postavení obratlů páteře, přispívat k současné optimální pružnosti a pevnosti všech kloubních spojení. Pohybová aktivita z pohledu primární prevence by neměla přetěžovat žádné složky podpůrně pohybového aparátu ani organismus jako celek. Cílem je přispět pohybovou aktivitou k úspěšné funkční i morfologické adaptaci na zátěž prostředím.
Nedostačující (a během života jedince většinou postupně se snižující) úroveň tělesné zdatnosti, vyplývající z nedostatečné pohybové aktivity se rozhodující měrou podílí na vzniku nejen metabolických, kardiovaskulárních a nádorových onemocnění, ale i na vzniku a rozvoji poruch podpůrně pohybového aparátu.
Pokud chceme docílit, aby námi doporučovaná pohybová aktivita byla „ individuálně optimální“, je nezbytné při její preskripci vycházet jak z aktuálního zdravotního stavu jedince, tak i z individuální analýzy stávající pohybové aktivity a funkčních i morfologických komponent zdravotně orientované tělesné zdatnosti.
Mezi funkční komponenty fyzické zdatnosti řadíme:
- kardiorespirační zdatnost (schopnost přijímat, transportovat a využívat kyslík)
- neuromuskulární zdatnost (svalová síla, flexibilita, kvalita základních posturálních a pohybových stereotypů)
Pro objektivní posouzení strukturálních (morfologických) komponent využíváme antropometrické a další metody, které slouží k vyhodnocování výživového stavu jedince.
Možnosti analýzy vybraných komponent zdravotně orientované tělesné zdatnosti a pohybové aktivity
Hodnocení úrovně pohybové aktivity a obecná doporučení pohybové aktivity
Sledování aktuální individuální úrovně pohybové aktivity zahrnuje zjištění typu, frekvence, intenzity a celkového objemu vykonávané pohybové aktivity. Údaje odebíráme anamnesticky, využíváme dotazníky. Nevýhodou anamnesticky získaných údajů je zkreslení skutečného přesného objemu vykonané pohybové aktivity: podhodnocení nebo nadhodnocení. Pro průběžné sledování a zpřesnění odhadu úrovně pohybové aktivity lze využít různé osobní pomůcky (např. krokoměry, akcelerometry).
Pro možnost mezinárodního porovnávání úrovně pohybové aktivity v populaci WHO vyvinula Global Physical Activity Questionnaire (GPAQ). Pomocí tohoto dotazníku sledujeme pohybovou aktivitu vykonávanou nejen ve volném čase (jako např. rekreační sport, práce v domácnosti apod.) ale i v zaměstnání a během transportu (chůze, jízda na kole do práce apod.) Sledována je pohybová aktivita (vykonávaná souvisle minimálně vždy 10 minut) za 7 dní a celkový objem vykonané aktivity je znázorněn v tzv. MET minutách. MET (metabolický ekvivalent) je jednotka používaná pro vyjádření intenzity fyzické zátěže. 1MET odpovídá klidové spotřebě kyslíku: tj. 3,5ml/kg/min, je ekvivalentem klidového metabolismu, tj. klidové energetické spotřeby organismu cca 1kcal/kg/hod. Čím je vyšší intenzita fyzické zátěže, tím vyšší jsou požadavky na energii nutnou k jejímu pokrytí. Např. pro hodnocení jedinců ve středním a pozdním dospělém věku je odhadováno, že spotřeba energie při pohybové aktivitě střední intenzity (př. chůze o rychlosti 5,5 km/hod) je 4x větší než v klidu, při pohybové aktivitě vysoké intenzity (př. jízda na kole 20km/hod) 8x větší. Čas strávený určitou aktivitou (v min/týden) je vynásoben příslušným energetickým ekvivalentem a výsledkem je celkový objem pohybové aktivity vyjádřený v tzv. MET minutách/za týden. Jako střední úroveň pohybové aktivity (a zároveň jako minimální doporučovaný celkový objem pohybové aktivity) je udáváno:
Pro dospělé:
600 MET minut za týden: tj. alespoň 150 minut pohybové aktivity střední intenzity za týden, provozovat pohybovou aktivitu je doporučeno nejlépe 3x až 5x/týden, souvisle vždy minimálně 10 min. Tato aerobní aktivita by měla být doplněna o cvičení zaměřené na posilování a protahování vybraných svalových skupin cvičení a cvičení zaměřená na prevenci vadného držení těla.(Pro starší 65 let je zvlášť zdůrazněna potřeba posilovacích cvičení a rovnovážných cvičení jako prevence úrazů).
Pro děti (5–17 let):
Minimálně 60 minut pohybové aktivity střední až vyšší intenzity denně. Pohybové aktivity mají být co nejpestřejší, rovnoměrně rozvíjející aerobní zdatnost i svalovou sílu a flexibilitu, obratnost a rovnováhu. Zásadou by měla být vždy prevence jednostranného zatěžování určitých svalových skupin při specializovaném tréninku a vždy kompenzace dlouhodobého trávení času ve statické poloze kompenzačním cvičením.
Posuzování kardiorespirační zdatnosti a individualizovaná doporučení optimální pohybové aktivity
Uvedená doporučení je třeba vždy korigovat s ohledem na celkový zdravotní stav jedince, na individuální úroveň výchozí tělesné zdatnosti. Zejména pro ženy starší než 50 let a muže starší než 40 let s žádnou nebo velmi nízkou úrovní pohybové aktivity a kteří mají další známé rizikové faktory kardiovaskulárního onemocnění (tj. např. obezita, kouření v anamnéze) či již prokázané kardiovaskulární nebo respirační onemocnění a/nebo poruchu pohybového aparátu může znamenat nevhodná pohybová aktivita zvýšené riziko ohrožení zdraví. Ale přísně individuálně plánovaná a kontrolovaná pohybová aktivita je součástí celkové léčby pacienta (kardiovaskulární a/nebo neuromuskulární rehabilitace).
Před preskripcí optimální pohybové aktivity zjistíme i stravovací zvyklosti. Doporučení týkající se úpravy energetického objemu i nutričního složení stravy by měla korespondovat s doporučovanou pohybovou aktivitou.
Vždy před preskripcí pohybové aktivity je třeba zvážit absolutní a relativní kontraindikace fyzického tréninku. Na odborném pracovišti (oddělení funkční diagnostiky, oddělení tělovýchovného lékařství, zátěžové laboratoře) by měly být vyšetřeny osoby se známými riziky kardiovaskulárního onemocnění a osoby s již diagnostikovaným kardiovaskulárním, plicním nebo metabolickým onemocněním. Provedení komplexního vyšetření a vyšetření kardiorespirační zdatnosti, tj. stanovení maximální kardiorespirační kapacity při zátěžovém spiroergometrickém testu na odborném pracovišti (přestože není povinné) je doporučováno i asymptomatickým osobám, mužům mladším než 40 let a ženám mladším než 50 let v případě, že byly déle než 3 roky inaktivní a plánují provozování systematické pohybové aktivity střední a vyšší intenzity. Jednak lze přesněji určit úroveň tělesné zdatnosti a efektivněji sestavit plán pohybové aktivity, jednak lze odhalit dosud klinicky němé nefyziologické stavy.
Před zahájením testů vždy zjistíme případné kontraindikace vyšetření, tj. např.: manifestní oběhová nedostatečnost; akutní zánětlivé onemocnění myokardu a další závažná kardiopulmonální a celková onemocnění.
Za optimální metodu pro hodnocení kardiorespirační komponenty tělesné zdatnosti a následné doporučení individuálně optimální intenzity pohybové aktivity (aerobní zátěže) je považováno zátěžové spiroergometrické vyšetření. Při tomto testu (při stupňované zátěži na bicyklovém ergometru, běhátku, popř. s využitím ručního rumpálu pro paraplegiky) lze vyhodnotit maximální aerobní kapacitu (tj. maximální spotřebu kyslíku: VO2max), objem vydechovaného oxidu uhličitého, poměr respirační výměny (mezi vydechovaným oxidem uhličitým a spotřebou kyslíku), dechovou frekvenci, celkovou ventilaci, dechový objem, nárůst krevního tlaku a srdeční tepové frekvence v průběhu zatížení, maximální srdeční frekvenci (tj. TFmax – nejvyšší hodnotu srdeční frekvence dosažené při maximálním zatížení v testu), koncentraci laktátu v krvi: aerobní a anaerobní práh. Zátěžový test je ukončen při dosažení subjektivního maxima zatížení, subjektivních potížích nebo při změnách na EKG, při neadekvátním zvýšení tlaku.
Parametr VO2max udává maximální množství kyslíku, které je vyšetřovaná osoba schopna transportovat z vnějšího prostředí, vstřebat a účelně využít na pokrytí energetických požadavků při pohybové aktivitě. Nad tento „práh“ zvyšující se zátěž již množství transportovaného a využitého kyslíku nezvyšuje. VO2max se vyjadřuje v ml O2/min/kg hmotnosti
Dosažené maximální zvýšení intenzity fyzické zátěže je udáváno i v příslušných násobcích jednoho metabolického ekvivalentu (1MET = klidová spotřeba kyslíku = 3,5ml O2/min/kg hmotnosti). Za vyhovující stupeň zdatnosti (u zdravých, mladých, asymptomatických jedinců) se považuje schopnost zvýšit klidovou spotřebu kyslíku minimálně 9x (tj. 9 METs).
Získané hodnoty jsou přesným ukazatelem kardiorespirační zdatnosti a umožní cíleně určit optimální intenzitu plánované pohybové aktivity. Pro udržení, respektive zvýšení kardiorespirační zdatnosti se doporučuje provozovat aerobní pohybovou aktivitu alespoň 3–5x/týden, délka zatížení v optimální „kardioprotektivní“ intenzitě by měla být cca 30 minut. Při zahájení pravidelné pohybové aktivity u jedinců po delší době inaktivity je doporučována zpočátku kratší doba zátěže a dolní hranice doporučovaného rozpětí intenzity zátěže. Doporučovaná optimální intenzita zátěže se udává v rozmezí 50–85 % VO2max (tj. 3,5–8 METs) dle trénovanosti, věku a limitujících rizikových faktorů. Optimální rozpětí intenzity zátěže lze stanovit i pomocí % tzv. rezervy tepové frekvence: RTF, přitom % RTF odpovídají % VO2 max.
Pro tento výpočet musíme znát:
- klidovou frekvenci (TFklid; změřenou ráno, ihned po probuzení, vleže)
- maximální tepovou frekvenci (TFmax; stanovenou reálně při zátěžovém testu nebo odhadnutou dle vzorce 220 - věk).
Procento rezervy tepové frekvence (např. 60 % RTF) vypočteme dle vzorce:
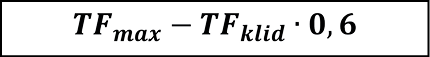
Výsledek připočteme ke klidové tepové frekvenci (tj. např. TF klid + 60% RTF) a získáme výslednou doporučovanou tepovou frekvenci. Tento výpočet je přesnější než obvykle udávané odhadované rozpětí optimální tepové frekvence (jen % z odhadnuté TFmax ) protože kalkuluje i s klidovou tepovou frekvencí, která je také závislá na trénovanosti jedince.
Orientačně lze vyhodnotit kardiorespirační zdatnost také pomocí vybraných terénních motorických testů. Ani tyto testy neprovádíme, jsou-li u vyšetřovaných přítomny uvedené kontraindikace a vždy máme-li pochybnosti o zdravotním stavu pacienta/klienta provedeme zátěžové vyšetření na odborném pracovišti.
Na základě zjištěných hodnot (zjištěné úrovně kardiorespirační zdatnosti) doporučíme individuálně optimální intenzitu a objem pohybové aktivity s ohledem na její očekávaný efekt. Základem je „sebekontrola“ tepové frekvence během pohybové aktivity, která umožní efektivní nastavení zátěže. Je-li hlavním cílem zvýšení kardiorespirační zdatnosti dospělého jedince podprůměrně zdatného (dosud delší dobu inaktivního) respektujeme pozvolné, postupné prodlužování „tréninkové“ jednotky (začínat na 5–10 min, přidávání po minutách, dosažení cca 30min), počáteční intenzitu zátěže doporučíme na dolní hranici kardioprotektivního pásma – tj.: TF klid + 50% RTF) a postupné zvyšování intenzity zátěže k horní hranici aerobního pásma. Je-li provozování pohybové aktivity součástí programu redukce hmotnosti, je doporučována střední intenzita zátěže (po postupném prodlužování a přidávání intenzity z lehké na střední, tj. opět cca TF klid + 50 % RTF) souvisle alespoň 40 minut, tak aby jako zdroj energie byl co nejvíce využíván tělesný tuk. Vždy je třeba pacienta upozornit, kdy musí okamžitě přerušit fyzickou zátěž (platí i pro okamžité přerušení testování zdatnosti): když ucítí bolest na prsou a/nebo vystřelující bolest do paží, šíje, čelisti, bude-li dušný, bude mít závrať a/nebo nauzeu, bude mít nepravidelný puls, pocítí nezvladatelnou svalovou slabost. Motivující pro pacienta/klienta je vedení tréninkového deníku a možnost kontroly zlepšující se zdatnosti.
Možnosti hodnocení neuromuskulární zdatnosti
Typ pohybové aktivity vybíráme vždy i s ohledem na neuromuskulární zdatnost a složení těla. Doporučení pohybové aktivity zaměřené na udržení resp. zvyšování kardiorespirační zdatnosti (tj. nejčastěji a nejsnáze dostupná chůze, popř. tzv. Nordic Walking – chůze s holemi, pro zdatnější jedince běh, popř. plavání, cyklistika) by vždy mělo provázet i doporučení vhodných kompenzačních cvičení. Tzn. uvolňovacích, protahovacích a posilovacích cviků sestavených dle typu provozované sportovní aktivity a zejména dle individuální analýzy posturální funkce podpůrně-pohybového systému, dle výchozí svalové síly a flexibility.
Zejména pro osoby s nadváhou a obézní jedince je nutné volit takové typy pohybové aktivity, které nebudou rizikově zatěžovat již tak nadměrnou hmotností přetížený podpůrně-pohybový systém. Pohybová aktivita je obézním obecně doporučována jako nedílná součást redukčního režimu. Snížení hmotnosti vede ke chtěnému odlehčení nosných kloubů a páteře. Odbouráním „tukového korzetu“ bez současného udržování svalové rovnováhy však může vzniknout chabé držení těla a následné funkční, popř. strukturální vertebrogenní algické syndromy.
Podpůrně-pohybový systém „ sedící“ populace je většinou přetěžován statickou zátěží (tj. dlouhodobým udržováním statických poloh) i bez ohledu na hmotnost a věk jedince. Proto by mělo alespoň orientační vyšetření posturální funkce podpůrně pohybového systému předcházet preskripci pohybové aktivity. Nesprávně zvolená, nadměrně anebo jednostranně zatěžující aktivita nejenže nepřinese očekávané pozitivní výsledky, ale může být i příčinou zhoršení nebo objevení se zdravotních potíží. Tyto pak bývají pro pacienta podnětem k přerušení snahy o zvyšování fyzické zdatnosti.
Před vlastním hodnocením posturální funkce anamnesticky zjistíme případné bolestivé či pohyb omezující stavy, poúrazové stavy, zaznamenáme i bolest spouštějící a provokující faktory, rodinnou zátěž.
Metody hodnocení postury
- aspektivní, somatoskopické metody (např. test držení těla dle Jaroše a Lomíčka, dle Matthiase, dle Kleina, Thomase a Maeyra, nutno počítat se subjektivní chybou vyšetřujícího);
- somatografické nezátěžové metody:
- optické metody: př. Moiré topografie,3D videotopografie,..
- dotykové metody: označení vybraných bodů na povrchu těla, poloha označených bodů se pak snímá dotykem snímacího hrotu (čidla) polohového snímače, výhodou je získání trvalého grafického záznamu, možnost grafické a numerické analýzy označených bodů (např. trnových výběžků obratlů) v třírozměrné kartézské soustavě, a možnost objektivnějšího porovnání stavu např. před a po pohybové intervenci;
- somatografické zátěžové metody (RTG, CT, MR).
Páteř je nosnou složkou umožňující vzpřímené držení těla, proto popisujeme zejména tvar a průběh páteře v předozadní i bočné projekci, sledujeme odchylky ve frontální, sagitální i axiální rovině, statiku páteře. Zajímá nás ale i postavení končetin (symetrie pánve, osy a délka dolních končetin), stabilita stoje, schopnost rovnovážného rozložení hmotnosti těla na končetiny (zvážení na dvou vahách: nefyziologický je stranový rozdíl větší než 5kg, u dětí předškolního a mladšího školního věku asymetrie větší než 10 % celkové hmotnosti těla), porovnání návykového stoje a aktivně vzpřímeného stoje a schopnost vydržet určitou dobu v této kvalitativně náročnější poloze. Již z typického postavení jednotlivých segmentů páteře, prohloubení popř. oploštění fyziologických křivek, z pozice hlavy a sklonu pánve můžeme usuzovat na hypoaktivitu na jedné straně a zároveň hyperaktivitu antagonistických svalových skupin. Svalové dysbalance dále podrobněji hodnotíme příslušnými svalovými testy, hodnotíme dynamiku páteře, správné funkční zapojení svalů do základních pohybových stereotypů, případnou hypermobilitu (flexe trupu, chůze, atd.). Důležité je i hodnocení dechového stereotypu (vleže na zádech by mělo převládat břišní dýchání, vsedě a vstoje dolní hrudní dýchání, nefyziologický je převažující horní typ dýchání, někdy pozorujeme i asymetrii dechové vlny).
Použité zdroje
Nutriční software NutriDan II: Nápověda, Jak postupovat.
Tomáš Pruša: Hodnocení nutričních software. Bakalářská práce. 2007. Lékařská fakulta Masarykovy univerzity Brno.
Eva Matoušková: Analýza stravovacích návyků pomocí programu NutriDan u hypertoniků. Bakalářská práce. 2010. Zdravotně sociální fakulta Jihočeské univerzity v Českých Budějovicích.
Literatura
National Research Council (U.S.) Subcommitee on the Tenth Edition of Tenth Edition of the RDAs, Food and Nutrition Board, Commission on Life Sciences. Recommended Dietary Allowances. National Academy Press, Washington, DC, 1989.
Institute of Medicine, Food and Nutrition Board: Dietary Reference Intakes for Thiamin, Riboflavin, Niacin, Vitamin B6, Folate, Vitamin B 12, Pantothenic Acid, Biotin, and Cholin. National Academy Press,Washington, DC,1998.
Commission of the European Communities 1993. Nutrient and energy intakes for the European Community. Reports of the Scientific Committee for Food ( Thisty –first series) Commission of the European Communities, Directorate-General Industry, Luxembourg.
SZO: FAO/WHO 1970. Requirements of ascorbic acid, vitamin D, vitamin B12, folate, and iron. Report of a joint FAO/WHO expert group, World Health Organ Tech Rep Se, No 452, ppl 75
FAO/WHO 1988. Requirements of vitamin A, iron, folate and vitamin B12, Report of a Joint FAO/WHO Expert consultation, FAO Food Nutr Ser, No 23, FAO, Rome.
WHO/FAO/IAEA. 1996. Trace elements in human nutrition and health, World Health Organisation, Geneva
Codex Alimentarius nutrient reference values (NRV) (FAO Codex Alimentarius 1995.
Potravinové tabulky, II. díl. Společnost pro výživu ve spolupráci s Ministerstvem zemědělství ČR, Praha 1993.
Fiala, J., Brázdová, Z., Kozina, V: Nová metoda hodnocení výživových zvyklostí. Hygiena 44, 1999, No. 1, p. 15-23.
U.S. Department of Agriculture and the U.S. Department of Health and Human Services. Ten-year plan for the National nutrition Monitoring and Related Research Program. Federal Register 58(111):32752-32806. June11,1993
Buzzard, I.M, Sievert, Z.A.: Research priorities and recommendation for dietary assesment methodology. AM J Clin Nutr, 1994, 59, s.275S-289S
Sealeman, A., Herrmann, D.: Memory from a broader perspective. New York, Mc Graw-Hill, Inc., 1994.
Frayn, K.N., Macdonald, I.A: Assessment of substrate and energy metabolism in vivo. In: Draznin, B., Rizza, R. (eds) Clinical Research in Diabetes and Obesity, Vol. 1, pp.101-124. Totoura, N.J: Humana Press. 1997
Recommended Dietary allowances, 10th edition. National Academy of Sciences, Published by the National Academy Press. 1989
Energy Expenditure in Humans: The influence of Activity, Diet and Sympathetic Nervous System, Ian A. Macdonald in Kopelman, P.G., Stock, M.J: Clinical Obesity. Blackwell Science. 1998.
Young, V.R., W.P.Steffee et al: Total human body protein synthesis in relation to protein requirementsat various ages, Nature 253;192 (1975).
Jeevanandam M, Lowry SF, Horowitz GD, Legaspi A., Brennan MF. Influence of increasing dietary intake on whole kinetis in normal man. Clin Nutr 1986;5:41-48).
Gurr, M.I., Fats, Human Nutrition and Dietetics (J.S. Garrow and W.P.T. James eds.) Churchill Livingstone, London, 1993, p.77.
Gurr, M.I., Role of fats in Food and Nutrition, Elsevier Applied Science Publishers, London 1992
Mattson, F.H., and S.M. Grundy, Comparison of dietary saturated, monounsaturated and polyunsaturated fatty acids on plasma lipids and lipoproteins in man. J. Lipid. Res. 26:194 (1985)
Nettleton, J.A., n-3 fatty acids: composition of plant and sea food sources in human nutrition. J. Am. Diet Assoc. 91:331 (1991)
HLÚBIK, P.: Vitamíny – důležitý faktor ovlivňující zdraví – 1. část: Metabolismus liposolubilních vitamínů. Interní medicína pro praxi, 2001, vol. 3, (č.11), s. 503-505.
Shenkin, A: Adult micronutrient requirements in: Payne-James, J., Grimble, G., Silk, D: Artificial Nutrition Support in Clinical Practice London. 2001
Lebl, J., Krásničanová, H.: Růst dětí a jeho poruchy. Galén, Praha 1996
Müllerová, D. a kol.: Obezita – prevence a léčba. Mladá fronta, Praha 2009.
Müllerová, D. a kol.: Hygiena, preventivní lékařství a veřejné zdravotnictví. Karolinum,Praha 2014.
Pařízová, J., Lisá, L. a kol.: Obezita v dětství a dospívání. Terapie a prevence. Galén, Praha 2007.
Růstové grafy: http://www.szu.cz/publikace/data/rustove-grafy
http://www.szu.cz/tema/podpora-zdravi/pohybova-aktivita
World Health Organization: http://www.who.int/
Barna. V. et al.: Manuál k vyšetření pohybového aparátu dítěte v ordinaci praktického lékaře, Praha, SZÚ, 2003.
Bursová, M.: Kompenzační cvičení – uvolňovací, protahovací, posilovací, Praha, Grada, 2005.
Janda, V.: Funkční svalový test. Praha, Grada/Avicenum, 1996.
Kolář, P.: Vadné držení těla z pohledu posturální ontogeneze. Pediatrie pro praxi 2002; 3; 106-109.
Kolisko, P. et al.: Hodnocení tvaru a funkce páteře s využitím diagnostického systému DTP-1,2. Olomouc, FTK UP, 2003.
Pastucha, D. et al.: Pohyb v terapii a prevenci dětské obezity. Praha, Grada/Avicenum, 2011