Otrava alkoholy (etanolem, metanolem, etylenglykolem)
| Stránky: | POSTUDIUM |
| Kurz: | Otrava alkoholy (etanolem, metanolem, etylenglykolem) |
| Kniha: | Otrava alkoholy (etanolem, metanolem, etylenglykolem) |
| Vytiskl(a): | Nepřihlášený host |
| Datum: | čtvrtek, 25. dubna 2024, 07.06 |
Popis
1. Otrava etanolem
S etanolem se člověk setkával odpradávna; jeho účinky na organismus jsou tedy obecně dobře známé. V další kapitole bude probráno vstřebávání etanolu, jeho metabolismus, stanovení v biologickém materiálu a následky akutní i chronické intoxikace. Obecně známé klinické příznaky akutní a chronické intoxikace etanolem nejsou obsahem textu. V kapitole 1.2 se jen krátce dotkneme dnes spíše zpochybňovaných příznivých účinků příjmu mírného množství etanolu.
Další alkoholy – etanol a etylenglykol – způsobují závažné otravy: metanol otravy náhodné, způsobené jeho záměnou za etanol, etylenglykol pak spíše otravy se sebevražedným úmyslem.
Etanol se vstřebává v celém trávicím ústrojí. Vstřebávání snižuje nízká teplota nápoje, vysoký obsah cukru v nápoji (váže na sebe vodu) a tučné jídlo (zpomaluje vyprazdňování žaludku). Naopak vstřebávání zvyšuje oxid uhličitý (perlivá vína, přídavek sodovky) a prázdný žaludek. Zanedbatelné množství se vyloučí nezměněné plícemi a močí, zbytek je v organismu metabolizován. Muži odbourají asi 1 gram etanolu, ženy 0,85 g/10 kg tělesné hmotnosti za hodinu; protože však ženy mají v průměru nižší hmotnost, odbourávají etanol výrazně pomaleji. Pomaleji odbourávají etanol i děti a starší jedinci, zejména s onemocněním jater.
Etanol je v organismu metabolizován v játrech; je oxidován do dvou stupňů – na acetaldehyd a kyselinu octovou (acetát). U člověka, který není na alkoholu závislý, se uplatňují dva na sebe navazující enzymy: alkoholdehydrogenáza (ADH) a aldehyddehydrogenáza (ALDH). Oba vyžadují koenzym NAD+, který je při oxidaci etanolu a acetaldehydu redukován na NADH. Alkoholdehydrogenáza se nedá opakovaným příjmem etanolu indukovat (a nelze tedy ani zvýšit rychlost odbourávání etanolu). Navíc se jedná o enzym nespecifický: katalyzuje i oxidaci jiných alkoholů, jako je metanol a etylenglykol. Poznatku, že afinita alkoholdehydrogenázy k etanolu je výrazně nejvyšší, se využívá k léčbě otrav těmito alkoholy – viz níže. Osoby mongoloidní rasy mají často mutaci genu pro aldehyddehydrogenázu, z toho plyne jejich snížená tolerance alkoholu. Inhibitor aldehyddehydrogenázy disulfiram (Antabus) se užívá k odvykací léčbě: v organismu se po jeho podání hromadí toxický acetaldehyd, který vyvolá nepříjemné příznaky, jako je zrudnutí, tachykardie, nevolnost, bolest hlavy a zvracení.
Alternativní cestou přeměny etanolu je tzv. mikrosomální etanol oxidující systém (MEOS). Má významnou úlohu u osob závislých na alkoholu. Nachází se rovněž v játrech a vede i ke stejným oxidačním produktům etanolu. Kromě enzymů se však liší i potřebný koenzym: je jím NADPH, který je oxidován za současné produkce superoxidového volného radikálu. To je jednou z příčin hepatotoxického účinku etanolu. Tento systém se dá opakovaným příjmem etanolu indukovat.
Obrázek 1.1 ukazuje obě cesty oxidace etanolu.
Obr. 1.1. Schéma oxidačního odbourávání etanolu v játrech
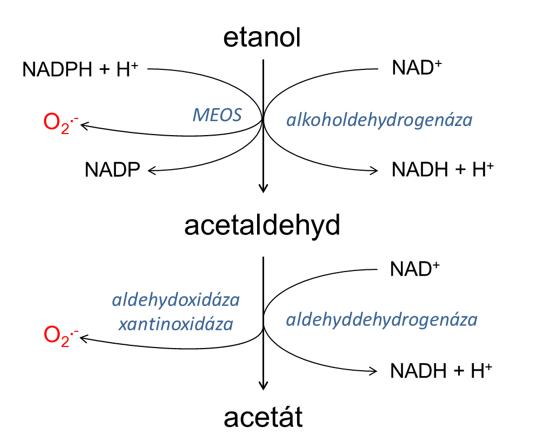
Požití většího množství etanolu kromě účinku na CNS vyvolá metabolickou acidózu, hypoglykémii, hyperurikémii, vzestup aktivity ALT a výrazný nárůst osmolality (etanol v koncentraci 1 g/l působí vzestup sérové osmolality asi o 22 mmol/kg). Otrava etanolem často doprovází jiné otravy, např. lékové, či požití drog. Příjem většího množství etanolu může být vyvolávajícím faktorem pro vznik akutní pankreatitidy.
Chronické požívání etanolu může vést k steatóze jater, protože v játrech probíhá zánětlivá reakce, hovoří se o alkoholové steatohepatitidě, která může progredovat do fibrózy a posléze až cirhózy jater s typickým laboratorním nálezem. Alkoholici mívají vyšší aktivitu γ-glutamyltransferázy (GGT) a zvýšený podíl bezsacharidového transferinu (carbohydrate-deficient transferrin, CDT), tj. transferinu se sníženým množstvím navázaných sacharidových řetězců. Protože na konci každého řetězce je navázána kyselina sialová, je CDT někdy nazýván mono- a disialotransferin. U některých alkoholiků se mohou projevit poruchy nutrice, zvýšený střední objem erytrocytů má vztah k nedostatku vitaminu B12, nedostatek vitaminu B1 může vést ke vzniku laktátové acidózy, která reaguje jen na suplementaci tímto vitaminem. Alkoholici mají obvykle poruchu metabolismu lipidů, zejména zvýšenou koncentraci VLDL; vysoký obsah triacylglycerolů v nich pak vede k chylóznímu vzhledu séra. Zvláště nebezpečný je příjem etanolu v těhotenství; postižení plodu se označuje jako fetální alkoholový syndrom.
Někdy je třeba ověřit, zda vyšetřovaná osoba pila alkohol před několika dny; v krvi je však již nulová hladina. Jedná se např. o kontrolu dodržování režimu při léčbě alkoholismu. V moči lze stanovit metabolit etanolu, etylglukuronid, obvykle imunochemickou metodou. Jeho zvýšené vylučování přetrvává 2 – 4 dny, v závislosti na množství přijatého alkoholu.
Stanovení etanolu je možné několika způsoby. Orientační je detekce ve vydechovaném vzduchu. K dispozici je množství přístrojů pracujících na různém principu – od levných a málo spolehlivých po sice drahé, ale poskytující věrohodný výsledek. V klinických laboratořích se etanol stanovuje obvykle spektrofotometricky s alkoholdehydrogenázou; tento způsob stanovení nevyžaduje speciální přístrojovou techniku a je dostatečně rychlý:
CH3CH2OH + NAD+ → CH3CHO + NADH + H+
Měříme pak nárůst absorbance při vlnové délce 340 nm, kdy absorbuje redukovaná forma pyridinového koenzymu (tzv. optický test).
Nejspecifičtějším způsobem je plynová chromatografie; dokáže rozpoznat i přítomnost jiných alkoholů, např. metanolu. Pro soudně lékařské účely se vyžaduje stanovení koncentrace etanolu dvěma nezávislými metodami, z nichž jedna musí být plynová chromatografie.
Titrační metoda podle Widmarka, založená na redukci dvojchromanu draselného na sloučeniny trojmocného chromu, se již neužívá – hodnotu zvyšovaly i jiné redukující látky obsažené v krvi.
Koncentrace etanolu v krvi (krevním séru) se tradičně vyjadřuje v g/l („promile“). Můžeme ji však vyjádřit i jako látkovou koncentraci; platí přitom vztah: 1 g/l = 22 mmol/l.
Na přítomnost alkoholu může upozornit i rozdíl mezi změřenou a odhadnutou osmolalitou, tzv. osmolální mezera (osmalal gap, osmolality gap). Postupujeme následujícím způsobem:
- Změříme osmolalitu séru.
- Odhadneme osmolalitu séra podle vzorce: 2 × Na+ + glukóza + močovina (vše v mmol/l).
- Spočítáme osmolal gap jako rozdíl změřené a odhadnuté osmolality.
- Výsledek vydělíme
22 a dostaneme koncentraci etanolu v g/l.
1.1. Orientační odhady koncentrace etanolu v krvi
V klinické praxi je často přínosné orientačně odhadnout, jakou hladinu etanolu pacient docílil po konzumaci různých alkoholických nápojů.
Na alkoholických nápojích je obsah etanolu obvykle uveden v objemových procentech. Protože etanol má menší hustotu než voda, hmotnostní procenta získáme vynásobením objemových procent číslem 0,8. Např. pivo „dvanáctka“ má 5 objemových procent etanolu, tedy 5 × 0,8 = 4 hmotnostní procenta. V jednom litru je tedy 40 g etanolu. Zjednodušeně můžeme říci, že:
- pivo obsahuje 3 % („desítka”) – 4 % („dvanáctka”) etanolu;
- víno obsahuje 10 % alkoholu (může se výrazně lišit);
- destiláty obsahují 40 % alkoholu (ale zde je odhad velmi nepřesný – jednotlivé nápoje se mnohou významně lišit, je třeba upravit dle konkrétního destilátu).
Etanol se velmi rychle a úplně vstřebává ze zažívacího traktu a distribuuje se v celkové tělesné vodě. Koncentraci etanolu v krvi po požití 1 litru piva „dvanáctky“ můžeme proto odhadnout jako 40 g v 60 procentech hmotnosti u mužů a v 50 procentech u žen. U 70 kg muže by tedy koncentrace etanolu byla 40/0,6 × 70 = 0,95 g/l. Reálná koncentrace je závislá na mnoha dalších faktorech – hlavně na rychlosti konzumace alkoholu, jeho teplotě, obsahu CO2 a konzumaci jídla, jak již bylo uvedeno v úvodu kapitoly. Pokles koncentrace etanolu v krvi je u občasného konzumenta alkoholu přibližně 0,15 g/l za hodinu; u „průměrného“ pacienta na akutním příjmu spíše 0,2 g/l za hodinu.
Při léčebném podávání etanolu u otravy etylenglykolem či metanolem uvažujeme obdobně. Obvykle aplikujeme bolusovou dávku etanolu a docílenou hladinu následně udržujeme kontinuální infuzí rychlostí, která odpovídá odbourávání etanolu. Abychom dosáhli např. koncentraci etanolu 1,2 g/l musíme 70 kg muži podat bolus 1,2 g × CTV, tedy 1,2 × 42 = 50,4 g. Pro udržení této koncentrace pak musíme pokrýt odbourávání etanolu – např. 0,2 g/l za hodinu, tedy podat 0,2 × 42 = 8,4 g za hodinu.
1.2. Existují příznivé účinky alkoholu?
Mnohé studie ukázaly, že alkohol požívaný v mírném množství může vykazovat příznivé účinky; patří k nim např. zvýšení koncentrace HDL-cholesterolu, snížení hladiny fibrinogenu a reaktivity krevních destiček; alkohol rovněž zlepšuje rozpustnost antioxidačně působících polyfenolů z piva a vína a usnadňuje tak jejich vstřebávání v tenkém střevě. Účinek mírného pití alkoholu je znám jako tzv. francouzský paradox – koncept formulovaný francouzskými epidemiology v 80. letech minulého století, totiž že ve Francii při stejném příjmu tuků je incidence kardiovaskulárních onemocnění menší než např. ve Velké Británii; důvodem měl být pravidelný příjem červeného vína s obsahem antioxidantů a samozřejmě i alkoholu. Objevily se však studie, které koncept francouzského paradoxu vyvracejí – kromě vína se liší i strava (vliv tzv. středomořské diety), navíc v různých zemích se posuzují kardiovaskulární onemocnění podle jiných kritérií. Někteří autoři ukazují i na to, že ve srovnávacích studiích byly mezi abstinenty někdy zařazeny i osoby, které přestaly pít alkohol právě ze zdravotních důvodů. Vliv alkoholu na kardiovaskulární onemocnění byl proto nejspíše nadhodnocen, zatímco negativní účinky příjmu alkoholu jsou nevyvratitelné.
2. Otrava metanolem
Otrava metanolem přichází sporadicky i v epidemiích. Metanol se nedá od etanolu odlišit vzhledem, chutí ani čichem, navíc bývá často s etanolem smíchán. Minimální toxická dávka je 0,1 mg/kg, letální dávka 1 – 2 mg/kg; při současném požití etanolu se tyto dávky významně zvyšují.
Metanol vyvolá příznaky podobné jako etanol, nebezpečný je toxický účinek jeho metabolických produktů: v organismu je působením enzymů alkoholdehydrogenázy a aldehyddehydrogenázy oxidován na formaldehyd a kyselinu mravenčí (formiát), která ireverzibilně poškozuje zrakový nerv (viz Obr. 1.2). Těžká metabolická acidóza je způsobena nejen kyselinou mravenčí vznikající oxidací metanolu, ale i hromaděním kyseliny mléčné – kyselina mravenčí totiž inhibuje cytochrom c oxidázu v mitochondriích. I metanol způsobuje vzestup osmolality krevního séra. Podezření na otravu metanolem (ale i etylenglykolem) vznikne při vysoké hodnotě osmolální mezery (osmolal gap) a negativní či výrazně nižší hladině etanolu, než by tomu odpovídalo.
Stanovení metanolu je možné plynovou chromatografií.
Obr. 1.2. Schéma oxidace metanolu na formaldehyd a kyselinu mravenčí
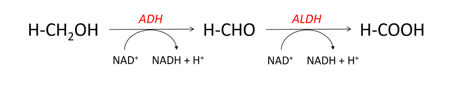
3. Otrava etylenglykolem
Etylenglykol je účinnou součástí nemrznoucí kapaliny Fridexu. Je často užívaný v sebevražedném úmyslu. I zde pozorujeme významný nárůst sérové osmolality. Etylenglykol je v organismu metabolizován na řadu metabolitů, mj. na relativně silné kyseliny glyoxalovou a šťavelovou. Opět se uplatňují stejné enzymy jako při oxidaci etanolu a metanolu (viz Obr. 1.3). Vzniká těžká metabolická acidóza, která prudce progreduje a ohrožuje život otráveného. Je dána vysokou koncentrací kyselin vzniklých oxidací etylenglykolu, ale i vyšší hladinou laktátu.
Obr. 1.3. Zjednodušené schéma oxidačního odbourávání etylenglykolu (toxické kyseliny zvýrazněny modře, ADH = alkoholdehydrogenáza, ALDH = aldehyddehydrogenáza)
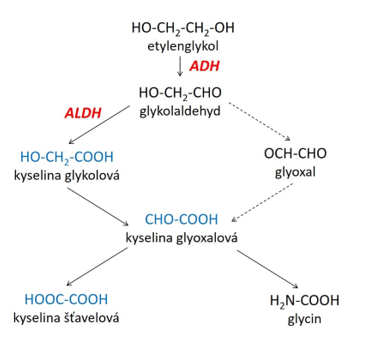
V moči může být záplava krystalů šťavelanu vápenatého (Obr. 1.4), jejich negativní nález však otravu etylenglykolem nevylučuje. Krystaly oxalátu vápenatého mohou vést k selhání ledvin, kyselina šťavelová tvorbou nerozpustného šťavelanu vápenatého snižuje koncentrace Ca2+ a hrozí křeče (tetanie).
Obr. 1.4. Krystaly oxalátu vápenatého v močovém sedimentu při otravě etylenglykolem
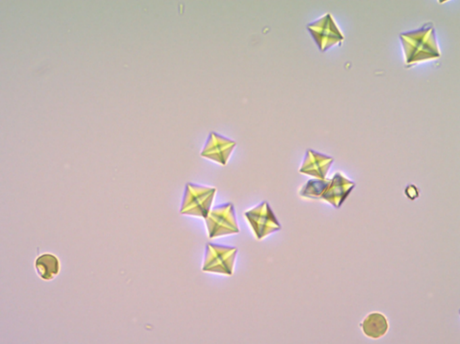
V poslední době bývá etylenglykol v nemrznoucích kapalinách nahrazován propylenglykolem. Ten nemůže být přeměněn na výše uvedené kyseliny jako etylenglykol, a je tedy méně toxický. Metabolizuje se na kyselinu mléčnou, proto při požití většího množství může vzniknout laktátová acidóza.
Stanovení etylenglykolu vyžaduje kapalinovou chromatografii a přípravu (derivatizaci) vzorku, není tedy běžné. Podezření na otravu etylenglykolem musí vzniknout, jestliže laktátová elektroda poskytne významně vyšší koncentraci laktátu než metoda spektrofotometrická. Při elektrochemickém stanovení laktátu totiž interferují oxidační produkty etylenglykolu, zejména kyselina glykolová a glyoxalová.
4. Léčba otravy metanolem a etylenglykolem
Je třeba co nejrychleji zahájit dialyzační léčbu k vyloučení alkoholů a jejich toxických oxidačních produktů; uplatní se i při úpravě metabolické a úpravě acidózy. Je nezbytné udržovat dostatečnou hladinu etanolu v krvi nemocného (1,0 – 1,5 g/l). Etanol má značně vyšší afinitu k alkoholdehydrogenáze než metanol či etylenglykol; enzym tedy přednostně oxiduje etanol a zpomaluje se vznik toxických metabolitů z metanolu či etylenglykolu (viz Obr. 1.5). Lze užít i inhibitor alkoholdehydrogenázy, 4-metylpyrazol (fomipezol), který je ještě účinnější.
Obr. 1.5. Schéma účinku alkoholu jakožto antidota při otravě metanolem a etylenglykolem; alkoholdehydrogenáza (ADH) přednostně oxiduje etanol a nevznikají modře zvýrazněné toxické oxidační produkty metanolu či etylenglykolu.
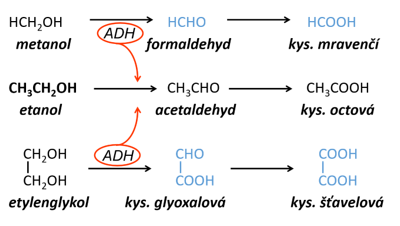
U otravy metanolem lze přidávat kyselinu listovou resp. její redukovanou formu (Leucovorin); je koenzymem enzymu, který oxiduje toxickou kyselinu mravenčí, i když značně pomalu. V případě otravy etylenglykolem prospívají thiamin a pyridoxin, jejichž deriváty tvoří koenzymy nutné pro alternativní přeměnu kyseliny glyoxalové na méně toxické produkty.
5. Doporučená literatura
- Beauchamp GA, Valento M. Toxic alcohol ingestion: prompt recognition and management in the emergncy department. Emerg Med Pract, 18(9), 2016: 1-20.
- Ferrières J. The Frech paradox: Lessons for the other countries. Heart, 90(1), 2004: 107-111
- Fillmore KM, Kerr WC, Ctockwell T, Chikritzhs T, Bostrom A. Moderate alcohol use and reduced mortality risk: Systematic error in prospective studies. Addiction Research & Theory, 14(2), 2006: 101-132
- Kruse JA. Methanol and ethylene glycol intoxication. Critical Care Clinics, 28(4), 2012: 661-711.
- Peterson K. Biomarkers for alcohol use and abuse. Alcohol Research & Health, 28(1), 2004/2005: 30-37.
- Scalley RD, Ferguson DR, Smart ML, Archie TE. Treatment of ethylene glycol poisoning. Am Fam Physician, 66(5), 2002: 807-13.